
货号:GC121001696
规格:10 RNX;20RNX;
价格:¥1650.00;2800.00;
产品用途:基因过表达或基因干扰的慢病毒的包装,以及后续稳转细胞株的构建,或直接用于动物体内注射
【产品概述】
基恩科(Gene carer)生物慢病毒包装试剂盒(Lentiviral Packing Kit)由优化的慢病毒包装辅助质粒混合物(Lentiviral Mix),高效转染试剂、慢病毒浓缩液,病毒感染增强剂四部分组成。适用于基因过表达或基因干扰的慢病毒的包装,以及后续稳转细胞株的构建,或直接用于动物体内注射。
【主要组成】
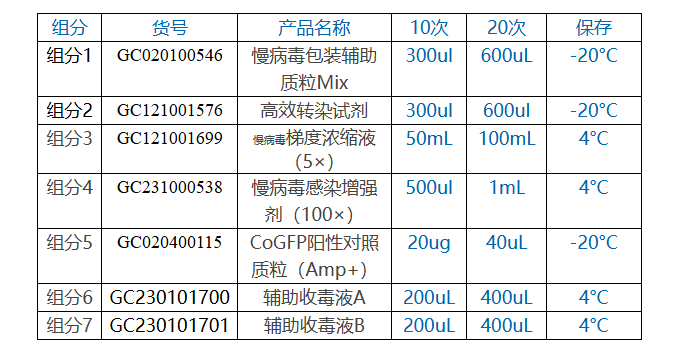
【自备试剂】:无菌水,PBS缓冲液,3%FBS+DMEM培养基,完全培养基:10%FBS+DMEM培养基
【收毒液配制】:收毒液:10%FBS+DMEM培养基+1%辅助收毒液A+1%辅助收毒液B(现配现用)
【运 输】:冰袋运输
【实验前准备及重要注意事项】
1.慢病毒表达载体:基恩科慢病毒包装试剂盒可以包装Plenti-,Plvx-,PCDH-等系列慢病毒表达载体,psiH1-,plk0.1-,Lenti-CRISPR等干扰或敲除表达载体。
2.表达载体质量:无内毒素提取慢病毒表达载体DNA,质粒DNA溶于无菌的TE或ddH2O中,以紫外光吸收法测定其浓度及纯度,保证所提质粒DNA 的A260/A280在1.8~2.0之间,浓度≥500ng/uL,质粒质量和浓度会影响慢病毒滴度。
3.细胞状态:良好的细胞状态对病毒的包装至关重要,避免细胞培养基有细菌、真菌或支原体的污染,尽量使用传代次数较少的细胞,如果细胞是刚复苏的话,传两代之后再进行病毒包装。
4.病毒包装转染前293T细胞汇合度约60%-70%最佳,细胞汇合度太低影响转染后细胞状态,汇合度太高影响转染效率。
5.包病毒后16-18h换液,否则转染试剂沉淀会降低病毒滴度。
6.滴度检测用荧光法、抗性法或我公司《滴度检测试剂盒》
【实验步骤】:以10cm培养皿为例
1)293T细胞分盘:转染前一天,将已经长好的细胞以合适比例传代到10cm培养皿中,当细胞长到60%-80%时准备转染。
2)转染前换液:转染前1~2h将需要转染的细胞换新鲜的培养基(3%FBS+DMEM培养基),10mL/10cm皿。(注意:293T细胞贴壁性不是很好,换液时应小心滴加尽量避免冲起细胞。
3)转染:取无菌的15mL离心管,加入1.5ml的基础培养基,按下列组分配制反应体系:

加入30ul高效转染试剂A液(组分2),混匀。室温放置15~20min后,均匀滴加到提前换过液的培养皿中,缓慢摇匀培养皿使转染试剂均匀分布后置于CO2培养箱中培养。
4)换液:转染18~20 h后,小心吸掉细胞培养液弃于盛有消毒液的废液杯中(注意:此时培养基中已含有少量的病毒,必须经处理后才能丢弃,所用的移液枪头等必须经消毒液浸泡处理后才能丢弃),加10mL收毒液继续培养。
5)病毒收集:换液24h后,吸取细胞上清液于50mL离心管(4℃保存),加10mL收毒液继续培养。换液24h后,吸取细胞上清液于前一次离心管中,4℃,500g离心5min,上清液用0.45μm滤器过滤后转移到新的离心管中,并确定过滤后病毒上清液体积。
6)病毒浓缩:将慢病毒梯度浓缩液(5×)按照1:4的比例添加到过滤后的病毒上清液中(如有20mL病毒上清液,则需要加5mL新慢病毒浓缩液),10,000 g 离心4小时。
7)吸弃上清或缓慢倒掉上清,可看到管壁病毒沉淀,收集病毒悬液,滴度检测。
8)滴度检测完成后,将病毒以40~50μL分装,保存于-80℃,备用。
