Seahorse 细胞能量代谢利用高灵敏度的细胞外氧气与H+流量变化检测技术,实时完成细胞内两条主要能量产生途径 —— 线粒体呼吸和糖酵解的测量,借助全自动药物加注装置,通过测定细胞外酸化率 (ECAR: Extracellular Acidificarion Rate ) 和氧气消耗速率 (OCR: Oxygen Consumption Rate )可以测得细胞有氧呼吸与糖酵解的基础水平、最高 / 最低水平及能量储备水平,从而绘制出完整的 " 压力曲线 " ,作为细胞能量代谢的黄金标准,已经广泛应用于肿瘤、糖尿病、神经退行性疾病、心血管疾病、免疫学研究、干细胞研究、药物发现与筛选等多个方向。
一、细胞能量代谢服务
1. 检测项目:直接测定各种代谢模式氧气消耗速率OCR和细胞外酸化率 Ecar 值,间接反应基础代谢率、最大呼吸率、呼吸储备能力、质子漏水平、产氧自由基、葡萄糖代谢、糖酵解能力、糖酵解储备能力、非糖酵解酸化等。
2. 主要检测样本:贴壁细胞、悬浮细胞、分离线粒体、组织微球等。
3. 检测周期: 1-3天
二、细胞能量代谢实验服务主要优势:
1. 专业的团队进行实验设计和实验数据分析;
2. 试剂耗材充足,满足各种实验需求,结果 可靠迅速;
3. 严格的质量控制体系,确保实验结果有效。
三、线粒体压力测试介绍:
线粒体压力测试实验通过依次加入线粒体电子传递链(ETC)的靶向药物测量细胞的氧气消耗速率( OCR )而得到反映线粒体功能的关键参数。该实验使用的药物为 oligomycin 、 FCCP 、 rotenone/antimycinA ,加入顺序及 ETC 靶点如图 2 ,药物作用原理如图 1 :
Oligomycin :该药物抑制ATP合酶(即复合物 Ⅴ ),在测量细胞基础呼吸后第一个加入,该药可以影响或降低通过 ETC 的电子流,引起线粒体呼吸或 OCR 减少,这部分减少的 OCR 与细胞 ATP 合成相关。
FCCP :该药在oligomycin后加入,是一种解偶联剂,加入该药会破坏质子梯度和线粒体膜电位,引起电子在 ETC 不受限制地传递,同时复合物 Ⅳ 的耗氧达到最大。 FCCP 刺激的 OCR 可被用来计算细胞备用呼吸能力(该值为最大呼吸与基础呼吸的差值),备用呼吸能力代表细胞对能量需求增加或在压力下作出反应的能力。
Rotenone/AntimycinA :第三次加入的药物,是rotenone和 antimycinA 的混合物。 Rotenone 是复合物 Ⅰ 的抑制剂, antimycinA 是复合物 Ⅲ 的抑制剂。这两种药物可关闭线粒体呼吸,从而能够计算出由线粒体之外活动所驱动的非线粒体呼吸耗氧。
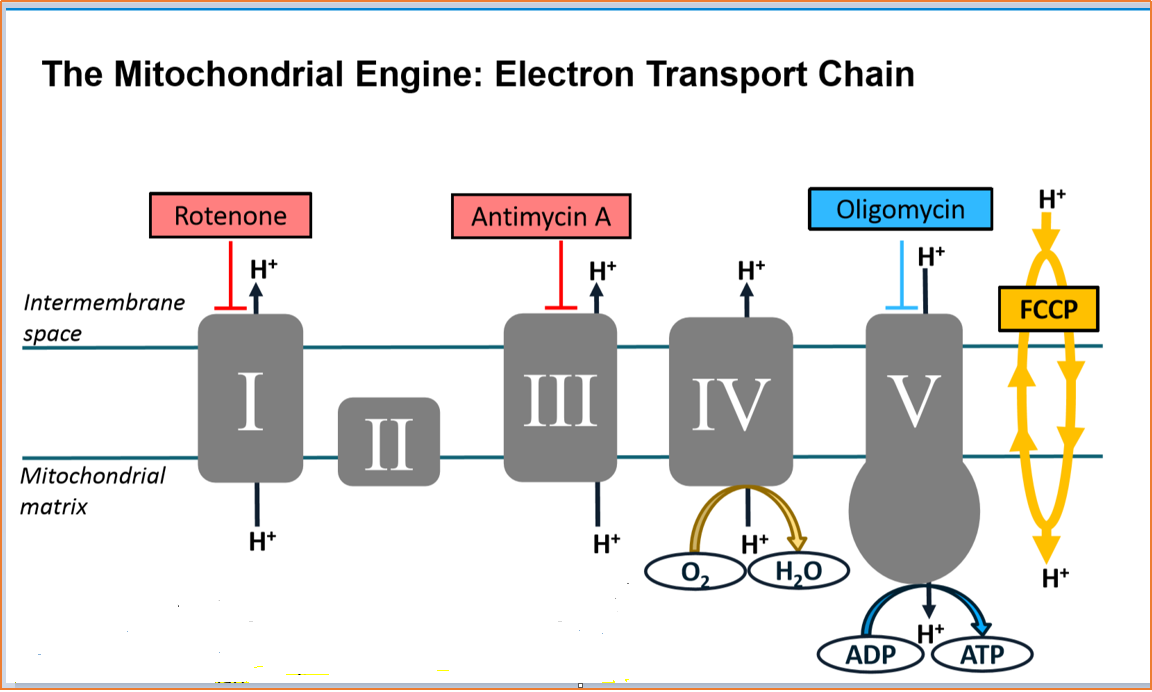
图1: 线粒体电子传递链

图2:标准OCR曲线
四、线粒体压力测试主要测量指标:
非线粒体耗氧量(Non-mitochondrial Respirarion):加入 rotenone 和 antimycinA 后仍持续的耗氧,这是由一部分细胞酶继续耗氧产生的,该参数对于精确测量线粒体呼吸功能非常重要。
基础呼吸速率(Basal Respirartion):用于满足细胞的 ATP 需求和质子漏的耗氧,代表细胞在基础状态下的能量需求。
ATP产生量( ATP Production ) : 加入 oligomycin 后产生的耗氧下降部分,占基础呼吸耗氧的一部分,用于驱动 ATP 合成,代表线粒体满足细胞能量需求的 ATP 合成能力。
最大呼吸速率(Maximal respiration):加入 FCCP 后获得的细胞最大耗氧, FCCP 通过刺激细胞呼吸链以最大能力工作,来模拟一种生理上的 “ 能量需求 ” ,这引起了底物(糖、脂肪、氨基酸)的快速氧化以应对这种代谢挑战,代表了细胞能够实现的最大呼吸速率。
呼吸储备能力(Spare Capacity ):最大呼吸减去基础呼吸的耗氧,代表细胞对能量需求的潜在响应能力以及细胞基础呼吸与理论呼吸最大值间的差距,细胞响应需求的能力可作为细胞适应性或灵活性的指标。
质子漏(H+( Proton) Leak ):基础呼吸减去 ATP 相关呼吸的剩余耗氧,该部分氧气消耗未偶联 ATP 合成。质子漏可作为线粒体损伤的标志,也可被认为是调节线粒体 ATP 合成的一种机制。
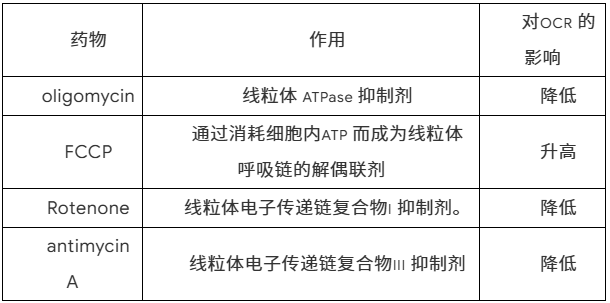
案例分析1: CD4+ T 细胞Ocar测定

图3: CD4+ T细胞 OCR 测定
五、糖酵解压力测试介绍:
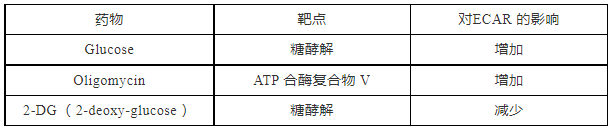
葡萄糖在胞浆中转化为丙酮酸,进一步转化为乳酸,并向细胞外环境中释放质子,引起胞外环境的酸化,本实验即测量细胞的胞外酸化率(ECAR )。需要注意,糖酵解压力测试实验的检测液中没有 glucose 和 pyruvate ,因此配制检测液时勿加入这两种底物。本实验通过依次加入 glucose 、 oligomycin 和 2-DG 来得到反映细胞糖酵解功能的参数如( 图4 )。

图4: 葡糖糖代谢和标准的ECAR曲线
Glucose :实验第一次加入的药物是饱和浓度的葡萄糖,细胞通过糖酵解途径利用该葡萄糖并将其分解为丙酮酸,产生 ATP 、 NADH 、水和质子。质子释放入胞外环境引起 ECAR 的迅速升高,这种由葡萄糖诱导的细胞应答被称为细胞在基础条件下的糖酵解能力。
Oligomycin:实验第二次加入的药物为 oligomycin , ATP 合酶的抑制剂,可抑制线粒体 ATP 产生,从而将能量产生转移至糖酵解通路,引起 ECAR 进一步升高,反映了细胞最大的糖酵解能力。
2-DG( 2-deoxy-glucose ): 2-DG 是最后加入的药物,该药通过竞争性结合糖酵解途径的己糖激酶而抑制糖酵解,引起 ECAR 降低从而证实实验中 ECAR 的产生来源于糖酵解途径。
六、糖酵解压力测试主要测量指标:
糖酵解( Glycolysis ):葡萄糖转化为丙酮酸的过程,本实验中加入饱和浓度葡萄糖后细胞达到的 ECAR 值,反映细胞在基础条件下的糖酵解能力。
糖酵解能力 (Glycolytic capacity):加入 oligomycin 后,细胞达到的最大 ECAR 值,指 oligomycin 有效关闭了氧化磷酸化功能后,迫使细胞利用糖酵解达到的最大产生能量的能力。
糖酵解储备 (Glycolytic Reserve): Glycolytic capacity 与 Glycolysis 的差值,反映了细胞满足能量需求的能力,以及糖酵解功能与细胞理论最大值之间的接近程度。
非糖酵解的酸化 (Non-glycolytic acidification ):细胞外酸化的其他来源,非来自糖酵解途径。
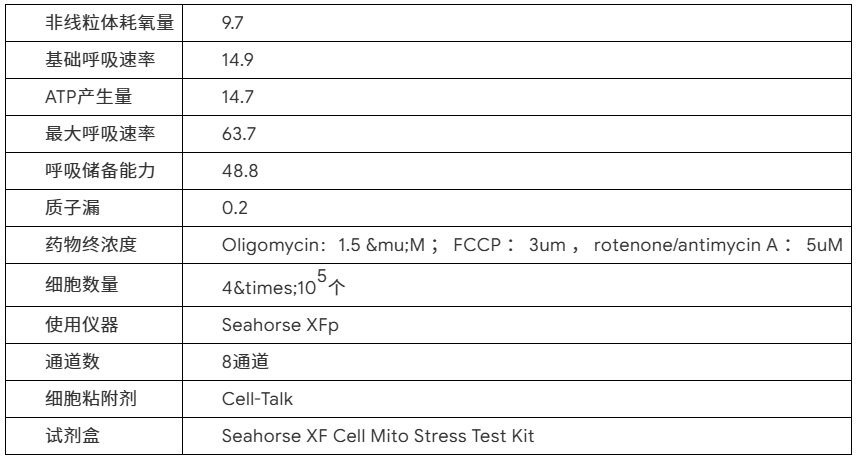
案例分析1: AGS 肿瘤细胞 ECAR 测定
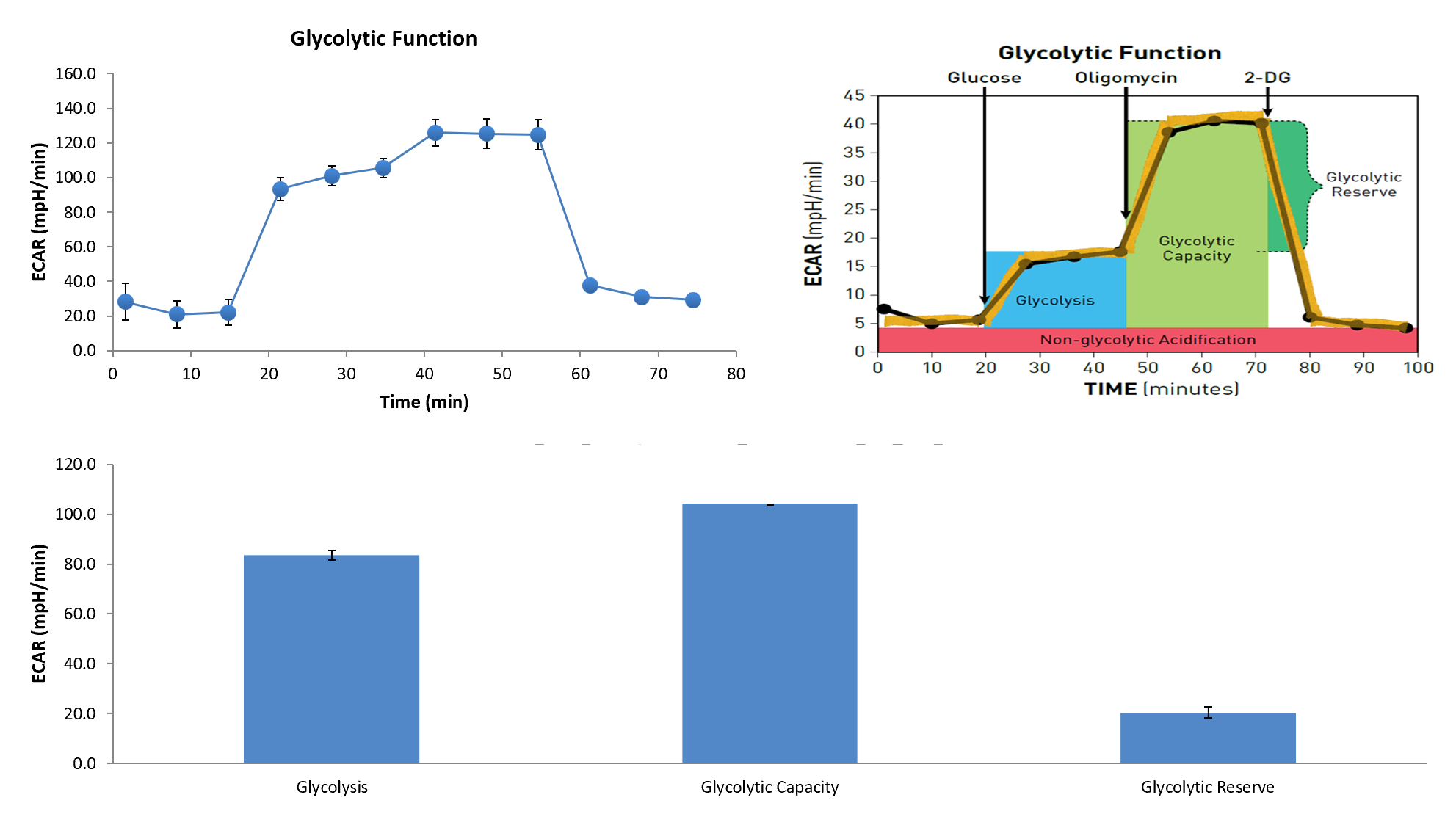
图5: AGS肿瘤细胞 ECAR 测定