哺乳动物细胞基因敲除采用CRISPR/Cas9系统转染目标细胞,通过抗性基因筛选获得相同表型的基因敲除细胞系,进一步通过挑取单克隆细胞扩增培养获得基因型相同的单克隆细胞株。我们具有丰富的哺乳动物细胞基因敲除经验,可为客户提供各种细胞的基因敲除以及单克隆细胞株的筛选服务。
一、 服务内容:
基因敲除方案的设计
CRISPR/Cas9敲除载体的构建
CRISPR/Cas9载体敲除效率的评估
CRISPR/Cas9载体目标细胞的转染
基因敲除细胞系的筛选
基因敲除细胞株的筛选
基因敲除细胞系/株的鉴定
二、服务流程
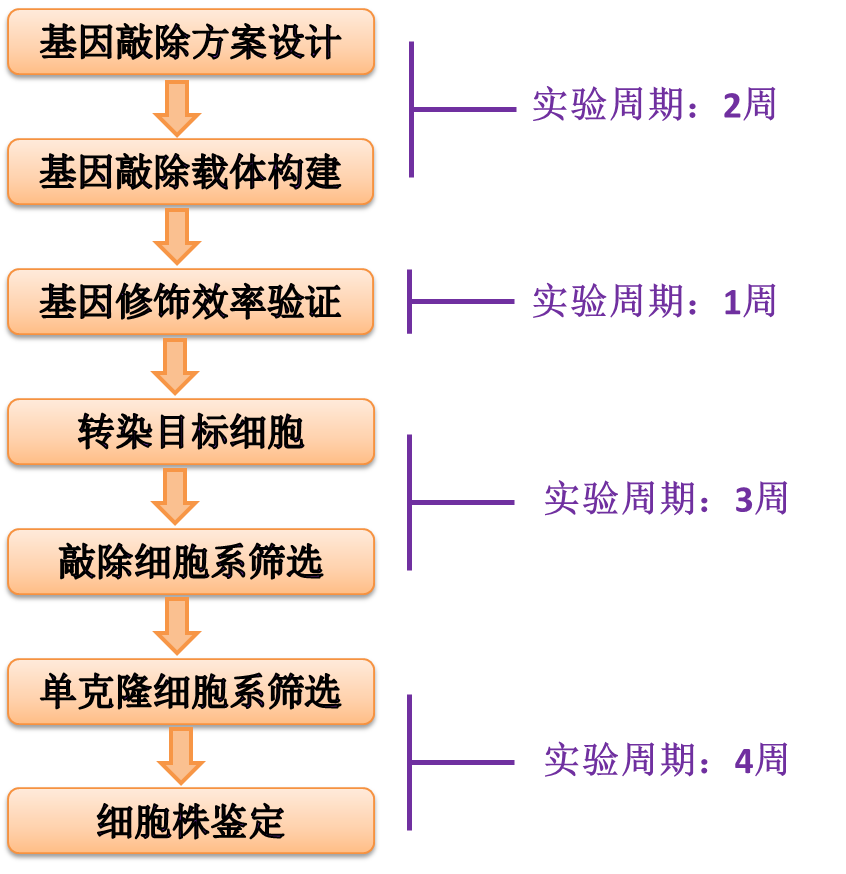
三、 技术路线:
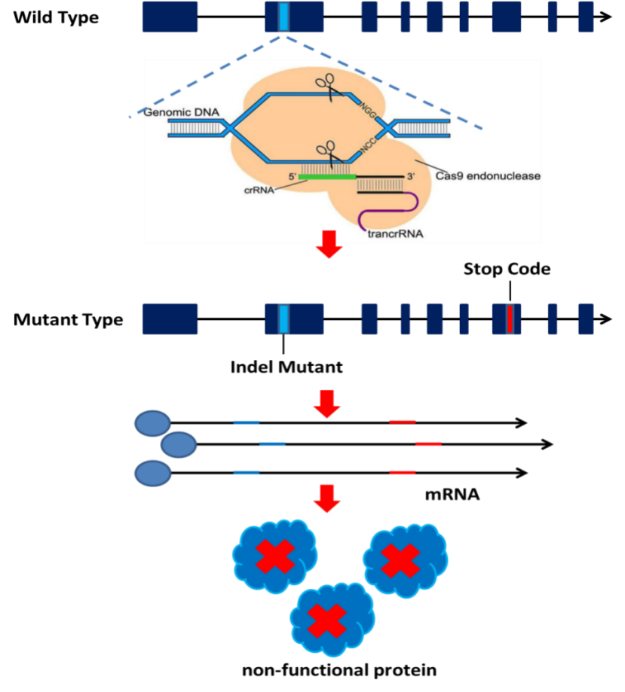
四、 交付内容:
1、实验报告内容:
基因敲除载体构建报告及测序结果
基因敲除细胞系/株筛选实验报告
基因敲除细胞系/株鉴定报告
2、产品内容:
基因敲除载体(质粒或菌液)
基因敲除细胞系或单克隆细胞株1-2株
3、其他:
目的细胞:肿瘤细胞系、干细胞、免疫细胞、原代细胞
构建周期:3-4周
材料提供:基因ID号、目的细胞、一抗(WB或流式)
转导方式:质粒、慢病毒、非整合慢病毒、腺病毒
五、案例分享
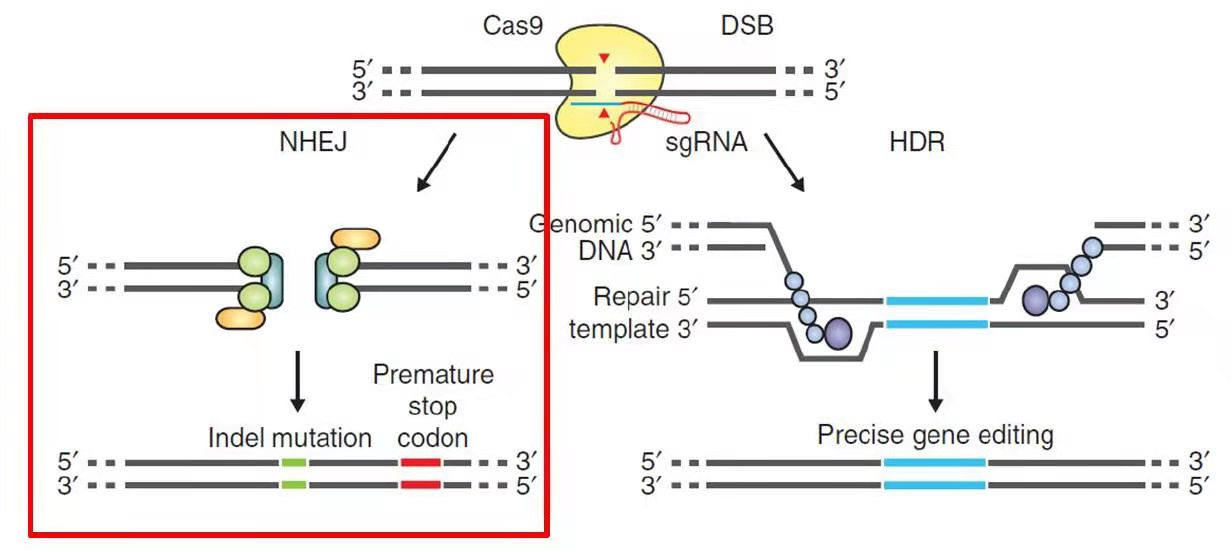
图1 CRISPR/Cas9介导的细胞内基因组DNA的修复过程
1.双gRNA/Cas9表达系统大片段基因敲除原理
在单gRNA/Cas9表达系统的基础上,再引入一个gRNA-Scaffold的表达盒,使其能够同时表达两个不同的gRNA靶向两个不同的序列。因此,针对目的基因的敲除,可设计针对该基因的两个不同靶点,这两个靶点之间的编码序列可以通过CRISPR/Cas-NHEJ通路完全敲除。
2.双gRNA/Cas9介导的基因敲除原则
具有两个靶点的双gRNA/Cas9系统可以针对基因的两个靶点进行切割,可以有效敲除长达1M的DNA序列,但是一般情况下,10kb以内基因片段敲除非常有效,也足以满足单个基因的敲除要求。具体设计要求如下:
2.1 如果目的基因比较小(小于10Kb或稍大于10Kb),可以设计将整个基因敲除,包括启动子序列;
2.2 如果目的基因很长,可以选择敲除其主要的几个外显子,也可以选择敲除部分编码序列和全部启动子序列;
2.3 如果有文献报道目的基因的敲除,按照文献敲除相同的序列和区域;3双gRNA/Cas9介导的基因敲除细胞系的构建
3.双gRNA/Cas9介导的基因敲除细胞系的构建
3.1 双gRNA/Cas9载体的构建
以lentiCRISPR(V2)载体为骨架,在原来的两个BsmBI酶切位点引入gRNA1-Scaffold-U6-gRNA2序列构建lentiCRISPR-Dual-Puro双gRNA/Cas9表达载体如图2所示:
.jpg)
图2. lentiCRISPR-Dual-Puro载体构建原理
3.2 双gRNA/Cas9载体基因敲除效率验证
(1)模式细胞转染:将293T细胞均匀的接种至12孔板中,待细胞汇合度达到80-90%进行细胞转染;注意:转染细胞可选择转染效率高的293细胞,小鼠细胞可选择MEF和3T3细胞;
(2)转染效率检测:转染后36-48小时,消化细胞提取细胞基因组,进行细胞基因型鉴定(PCR检测),如果敲除的PCR条带明显且亮度较强,说明这两个gRNA敲除效果明显,可用于目标细胞的基因敲除。
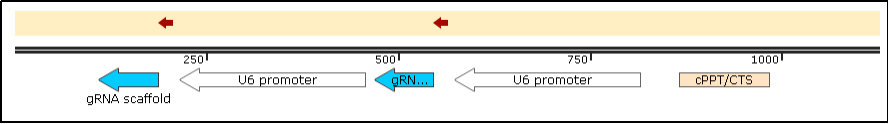
B2M基因敲除双gRNA/Cas9(lentiCRISPR-dual gRNA)图谱
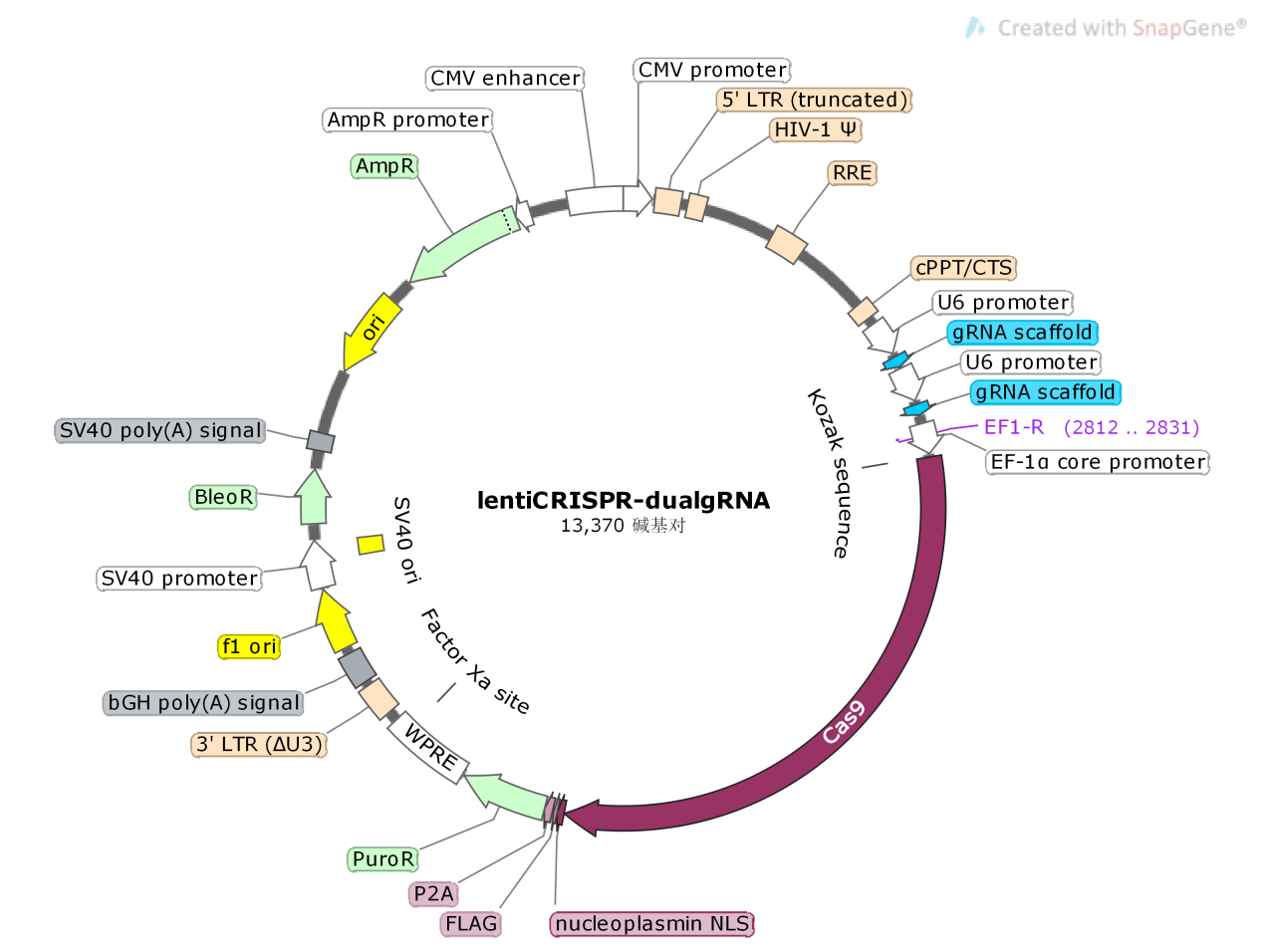
B2M基因敲除双gRNA/Cas9载体构建blast分析(红色箭头为gRNA序列)
(2)B2M基因敲除技术原理
B2M基因有4个外显子,其中前3个外显子为编码序列,故在第一个外显子上游和第三个外显子下游设计gRNA序列,基因型PCR检测引物设计在两个gRNA序列的外侧如下图所示:
(3)293T细胞B2M基因敲除细胞系构建
.jpg)
如以上细胞转染步骤将lentiCRISPR-dual gRNA转染293T细胞(6孔板),转染后48小时更换抗生素筛选培养液(2.5ug/ml嘌呤霉素),连续筛选5天,对照组细胞已完全凋亡,实验组细胞逆抗性增殖扩增。分离部分细胞,裂解,PCR检测结果如下:
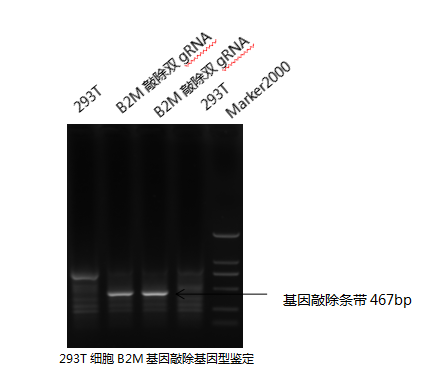
如上图293T细胞B2M基因敲除基因型检测,野生型条带4.6Kb未检测到,敲除型条带为467bp,经胶回收连接pMD18T载体,测序确定B2M基因的1、2和3外显子被完全敲除(如下图2个阳性T克隆的比对分析)。
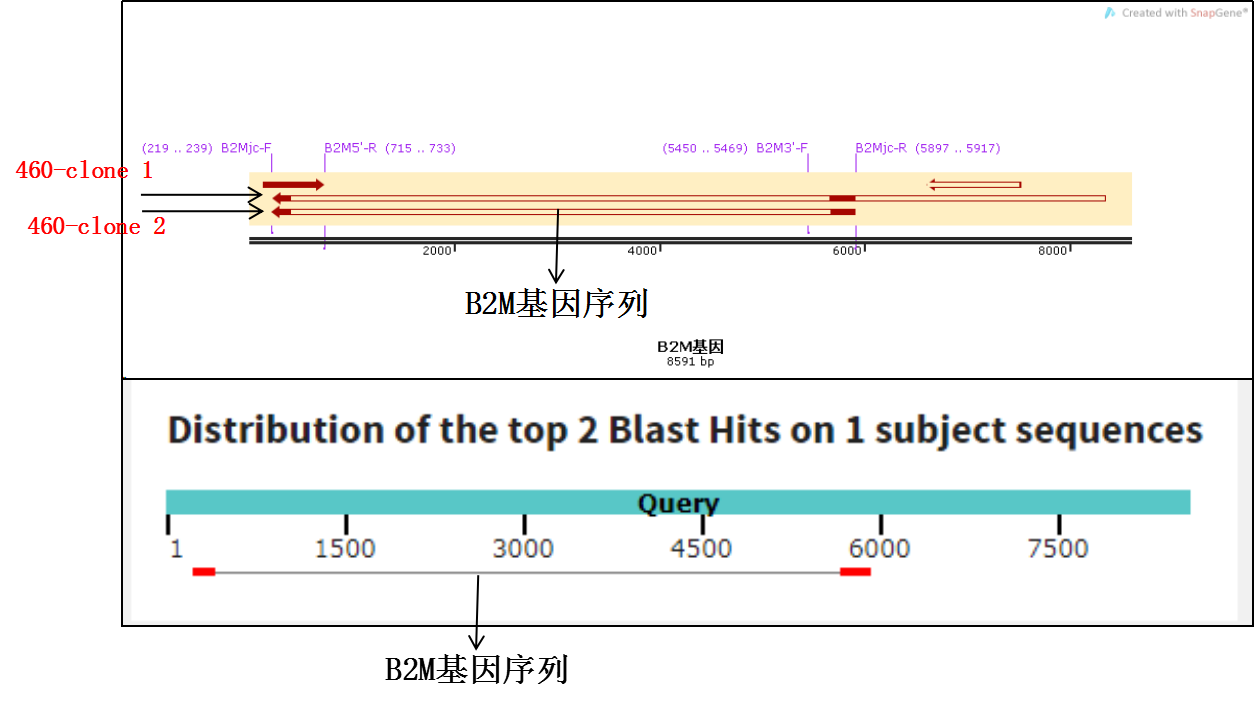
293T细胞B2M基因敲除测序分析