
Prime Editing(先导编辑)自2019年问世以来,因其能够精准实现碱基替换、小片段插入和删除,成为基因编辑领域的新大陆。但这片新大陆自从被发现以来就不是非常完美,从而开启了一场编辑优化的接力赛。首先,Prime Editing 编辑的效率可变且普遍较低,在不同基因组位点、不同细胞类型间效率差异巨大(从<1%到>50%),难以预测和掌控。其次,编辑过程中可能产生indel副产物(如由于DNA flap过长时间存在)或产生非预期编辑(如部分逆转录模板的整合)。对大片段插入效率极低,虽然理论上可行,但插入超过100 bp的片段效率急剧下降,远低于针对小片段的替换和删除。并且细胞状态影响编辑结果,错配修复活跃的细胞(如癌细胞)会"纠正"编辑结果,降低效率;非分裂细胞中的编辑效率通常低于分裂细胞。以及大尺寸复合物的体内递送困难等各种急需解决的问题,限制了应用。为此,研究人员从多个层面提出了优化策略,核心方向包括改造编辑器本身、优化引导RNA、调控细胞内在环境及利用人工智能辅助设计。
一. Prime Editing(先导编辑) 的基本原理:
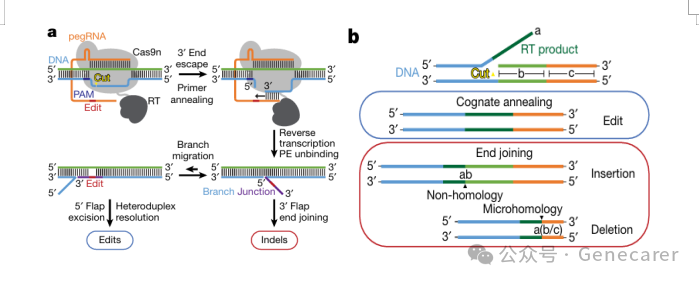
1.传统的Prime Editing包括三部分组件:一个是被改造过的Cas9“切口酶”(Cas9 Nickase, Cas9n),另一个是逆转录酶(Reverse Transcriptase, RT)和一条精心设计的“先导编辑引导RNA”(Prime Editing Guide RNA, pegRNA)。
Ø改造的Cas9酶 (Cas9 nickase, nCas9):Cas9酶原本含有两个可切割DNA序列的核酸酶结构域,即切割非靶链的 RuvC结构域和切割靶链的HNH结构域。通过引入H840A替换(将第 840位的组氨酸替换为丙氨酸),使Cas9酶 的HNH结构域失活,此时只有RuvC结构域发挥功能,其只能切割DNA双链中的一条链,避免了因双链断裂引发的不可预测的、有害的染色体变异,同时保留了其精准的定位和单链切口能力。
Ø同时在Cas9酶上融合了莫洛尼鼠白血病病毒(M - MLV)逆转录酶:当Cas9发生切割产生DNA单链断裂,暴露的单链3‘与pegRNA的PBS区结合M – MLV RT就以此为引物逆转录生成编辑链。(图a)
ØpegRNA:识别待编辑目标核苷酸序列,并编码用于替换目标序列的新遗传信息。pegRNA 由一个扩展的单向导RNA(sgRNA)构成,其中包含引物结合位点(PBS)和逆转录(RT)模板序列。在基因组编辑过程中,PBS 允许带切口的 DNA 链的 3' 端与pegRNA 杂交,而 RT 模板则作为合成编辑后遗传信息的模板。
2.编辑过程:首先是定位与切口,在pegRNA的引导下,Cas9n蛋白精准的寻找并定位到目标位置上发生精准的切割,形成一个“单链切口”(nick),这个操作远比剪断双链温和得多。其次是模板置换与转录,被切开的DNA单链(3'端)会从双螺旋中释放出来,并与pegRNA上的“RT 模板结合。此时,逆转录酶RT以pegRNA为模板,将被切开的DNA链作为引物,开始合成一段带有正确信息的新DNA序列。最后一步是整合与修复,新合成的、携带编辑信息的DNA链(即编辑后的3'新链)需要嵌入回原来的DNA双螺旋结构中,并取代表达原始信息的那条链(即竞争中的5'旧链)(图a)。随后,细胞自身的DNA修复系统会介入,将另一条未被编辑的链也修正过来,从而永久地将新信息固定下来。(图b)
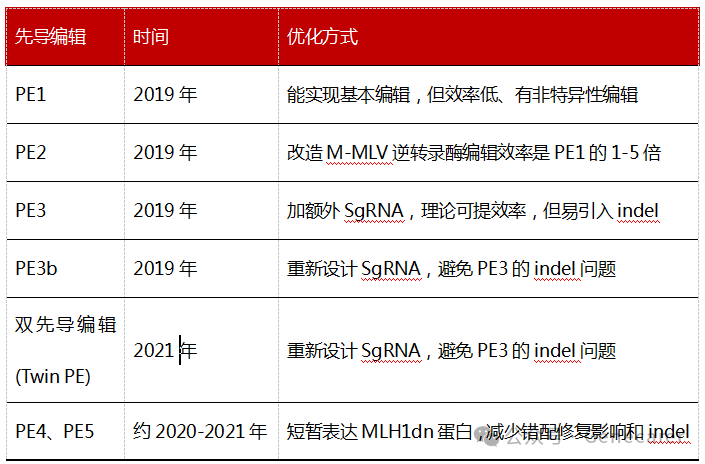
自Prime Editing(先导编辑)问世以来,PE编辑器从不同方向进行优化先后产生了PE1、PE2、PE3、PE3b、Twin PE、PE4、PE5、PEmax、PE7、uPEn和vPE等。
三. Prime Editing的优化策略和最新成果
1.下表概括了主要的优化策略:
优化维度 | 核心策略 | 代表方法/技术 | 主要效果 |
编辑器工程改造 | 改造Cas9-nickase,促进编辑链整合 | vPE编辑器 | 大幅降低indel错误(编辑: indel比例最高达543:1),提升产物纯度 |
pegRNA优化 | 优化引物结合位点(PBS)和逆转录模板(RT模板)设计 | PlantPegDesigner平台 | 通过控制PBS的熔解温度(~30°C)等参数,系统提升植物中编辑效率 |
调控细胞环境 | 抑制错配修复(MMR)通路 | MLH1小分子结合体(MLH1-SB) | 在HeLa细胞中相比PE7效率提升2.5倍,在小鼠体内提升3.4倍 |
调控细胞环境 | 招募表观遗传调控因子,提高染色质可及性 | 招募转录因子P65 | 改变目标区域染色质开放性,从而提高编辑效率 |
调控细胞环境 | 激活靶基因的转录 | CRISPR激活(CRISPRa) | 预激活基因表达,可将某些位点编辑效率从5%提升至66% |
系统设计与递送 | 使用双pegRNA同时靶向目标位点的两条DNA链 | 双pegRNA策略 | 在水稻内源位点,效率平均提升3.0倍 |
2. Prime Editing编辑优化的最新进展
近年来,随着对Prime Editing编辑的深入研究和AI技术在生物方面的应用,使得Prime Editing 的优化不只是局限编辑器本身,而是更加系统的契合了细胞内部的修复机制和编辑环境,一系列的大分子物质被发现并应用到PE系统极大的提高了编辑效率。下文列举了一些近两年具有突破性和代表性的例子。
(1)La蛋白保护pegRNAs促进了不同类型Prime editor在不同的内源基因位点和细胞类型中的编辑效率
原文链接:https://doi.org/10.1038/s41586-024-07259-6
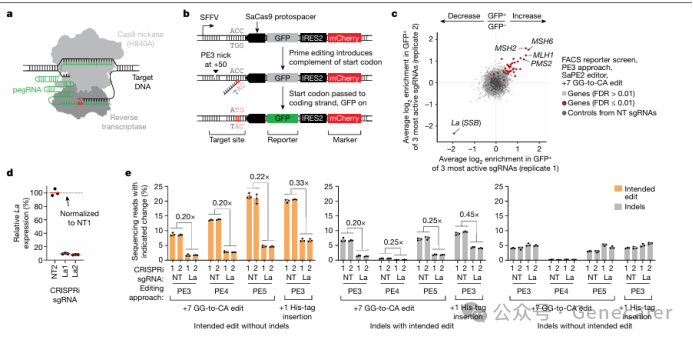
2024年4月3日,Nature在线发表了美国普林斯顿大学Britt Adamson、Lance R. Parsons团队的最新研究成果:“Improving prime editing with an endogenous small RNA-binding protein” 。该研究通过基因组规模的CRISPR干扰(CRISPRi)筛选,研究者们发现了一个关键的Prime editing促进因子——小RNA结合的外切核酸酶保护因子La。研究表明La蛋白通过其N端结构域与pegRNAs的3' polyU序列结合,从而促进Prime editing。La蛋白的这种作用对于不同类型的编辑(替换、插入、删除)和不同的细胞类型都是有效的。基于该发现,研究人员开发了一种新的Prime editor蛋白(PE7),该蛋白将La的RNA结合N端结构域融合到PEmax编辑器上。PE7编辑器在使用表达的pegRNAs和工程化pegRNAs(epegRNAs)以及为La结合优化的合成pegRNAs时,都能显著提高Prime editing的效率。
(2)效率远超PE7,Indel错误率降低60倍的vPE
原文链接:https://doi.org/10.1038/s41586-025-09537-3
改造PE编辑器蛋白的核心思路是优化编辑器与细胞内DNA修复机制的互动。在Prime Editing 编辑过程中新合成的3'链与它在双螺旋中的互补链存在一些碱基不匹配(因为包含了编辑信息),而那条等待被替换的5'旧链,则与互補链是完美配对的。根据化学热力学的基本原理,完美匹配的结构远比存在错配的结构更稳定。通过改造Cas9蛋白,让它对5'旧链末端的“钳制”变得松弛一些,或许可以显著增强的5'旧链末端降解,使编辑更容易被保留,从而在提高效率的同时,显著降低了有害的indel错误。基于此,2025年9月17日,Nature在线发表了麻省理工学院Robert Langer、Phillip Sharp的重磅研究:“Engineered prime editors with minimal genomic errors”。该研究通过对引导编辑器核心Cas9蛋白的精巧改造,从根本上将PE编辑的edit:indel比率提高到惊人的543:1,解决了indel的难题,开发出了一款兼具高效率与超高精准度的新一代引导编辑系统(vPE)。
首先,对Cas9蛋白DNA结合区域的氨基酸进行突变,并评估两个关键指标:一是切口位置的“松弛度”(Nick Shift Frequency);二是DNA末端的降解程度(DNA End Degradation)。他们发现,这两个指标之间存在着极强的正相关性。获得了一系列Cas9突变体(R780A、K810A、K848A和H982A等)在表现出更高的切口松弛度的同时,显著增强的5'旧链末端降解。设计了pPE将“编辑:错误”的比率(edit:indel ratio)提升高达28倍,但在一定程度上牺牲了编辑效率。
为此研究人员在pPE的基础上,又整合了另外几个能够增强Cas9活性的突变(如R221K和N1317R等),开发了xPE。xPE不仅完全恢复了pPE损失的效率,并且将“编辑:错误”比率进一步提升至354:1。
对cas9的改造可能会影响pegRNA的稳定性,因此研究人员又将目光投向PE7的编辑器,它通过引入一个名为“La”的RNA结合蛋白,像保护套一样将pegRNA保护起来,能够显著提升了编辑效率,最终开发了vPE,。与PE7仅为138:1的平均“编辑:错误”比率相比vPE的平均“编辑:错误”比率达到了 465:1。
(3)AI设计MLH1结合蛋白高效提升的prime editing效率
原文链接:https://doi.org/10.1016/j.cell.2025.07.010
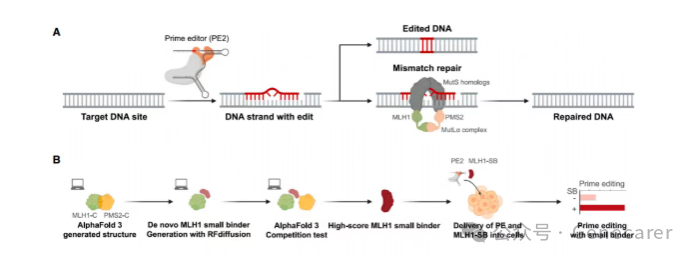
PE效率受限于细胞内DNA错配修复(MMR)系统——MMR会识别并修复PE引入的杂合碱基,显著降低预期编辑的保留率。2025年8月5日,Cell在线发表了首尔国立大学SangsuBae团队的最新研究进展:“AI-generated MLH1 small binder improves prime editing efficiency”。 该团队通过RFdiffusion与AlphaFold 3等AI工具设计出全新的小型MLH1结合蛋白(MLH1-SB),这种长度为82个氨基酸的蛋白能够结合到MLH1和PMS2的二聚体界面,从而破坏错配修复复合物MutLα的形成,极大提升prime editing编辑效率。值得注意的是,MLH1-SB表现出与多种先导编辑架构的良好兼容性,包括PE2、PEmax、PE6和PE7。
总的来说,Prime Editing的优化已经从一个点的突破,发展为蛋白质工程、RNA设计、细胞生物学与人工智能相结合的系统性工程。未来的趋势将是这些策略的更深度整合,以及针对特定应用场景(如临床治疗、农业育种)的定制化解决方案。
Jun Yan et al.Improving prime editing with an endogenous small RNA-binding protein. Nature, 2024, doi:10.1038/s41586-024-07259-6.
Chauhan, V.P., Sharp, P.A. & Langer, R. Engineered prime editors with minimal genomic errors.NaturE (2025).https://doi.org/10.1038/s41586-025-09537-3
Park JC, Uhm H, Kim YW, Oh YE, Lee JH, Yang J, Kim K, Bae S. AI-generated MLH1 small binder improves prime editing efficiency. Cell. 2025 Aug 1:S0092-8674(25)00799-8.doi: 10.1016/j.cell.2025.07.010. Epub ahead of print. PMID: 40769155.
我司可提供Primer Editor pegRNA 载体构建、PE3载体构建(一套)、TwinPE 载体构建、以及Lenti-PE-gRNA慢病毒包装、PE3b-腺病毒包装、Twin-PE-腺病毒包装、点突变细胞珠的构建
