美国纽约州立大学布法罗分校(University at Buffalo, State University of NYork)的化学与生物工程系Sriram Neelamegham团队发明基于SARS病毒颗粒VLP递送mRNA的新机制,并优化了包装VLP包装方法,3质粒系统即可高效包封VLP
研究通过分子工程优化了SARS-CoV-2病毒样颗粒(VLP)作为mRNA递送平台。开发了三质粒(3P)和双质粒(2P)系统,显著提高了病毒进入效率。通过更换不同病毒的糖蛋白(如SARS、MERS、VSV-G),可调控VLP的细胞趋向性。VLPs可包装多个转基因(最多四个),并成功递送功能性Cas9 mRNA实现基因编辑。此外,研究还证实了VLPs在小鼠肺部进行mRNA递送的可行性。
一、文章介绍
图1:比较4P与3P SARS2 VLPs的性能。3P系统使用更少的质粒,但病毒进入效率提高约7倍,结构蛋白表达更均匀,mRNA包装量更高。
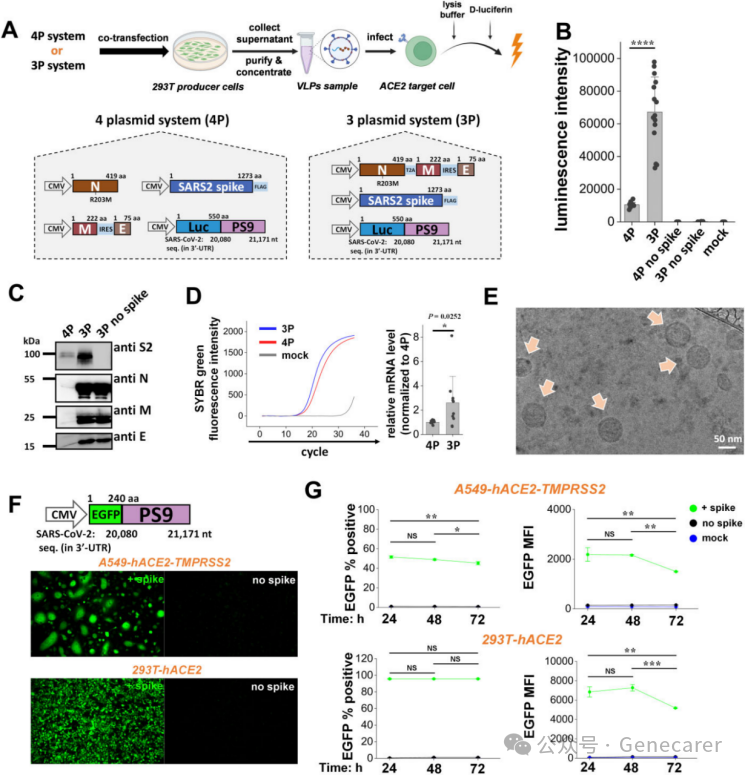
三质粒(3P)SARS2 VLPs优于四质粒(4P)系统
(A) 通过将四个或三个质粒共转染至293T生产细胞中,分别制备了4P和3P SARS2 Luc-PS9 VLPs。这些质粒编码病毒结构蛋白,以及连接有PS9包装信号的荧光素酶报告基因(Luc-PS9)。
(B) 荧光素酶检测显示,在293T-hACE2细胞中,使用3P VLPs相比4P VLPs,其发光强度高出约7倍。
(C) 将VLP浓缩液(M和E蛋白加样10μl,S2和N蛋白加样2μl)加入各泳道。蛋白质印迹分析表明,所有SARS2结构组件均被整合到VLPs中,且3P SARS2 Luc-PS9 VLPs显示的蛋白条带强度高于4P VLPs。
(D) RT-PCR结果显示,3P SARS2 Luc-PS9 VLPs中的Luc-PS9转录本水平更高。
(E) 3P SARS2 Luc-PS9 VLPs的冷冻透射电镜图像显示,其为球形的、约100纳米大小的VLPs,具有双层膜结构。
(F) 携带EGFP报告基因的3P SARS2 EGFP-PS9 VLPs能有效感染293T-hACE2和A549-hACE2-TMPRSS2细胞。荧光图像在感染后24小时采集。
(G) 流式细胞术检测VLP进入的时间进程表明,3P SARS2 EGFP-PS9 VLPs的荧光信号在24小时达到峰值,随后随时间延长而减弱。这一现象在293T-hACE2和A549-hACE2-TMPRSS2细胞中均被观察到。
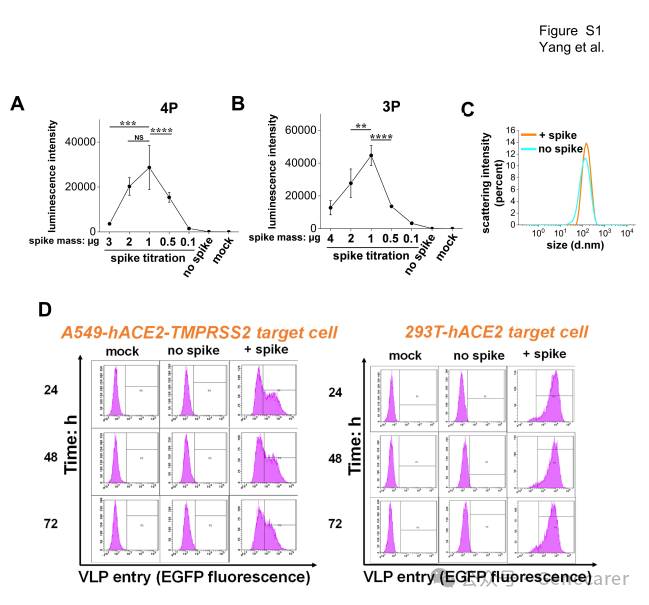
图S1. VLP 系统需要特定的刺突蛋白质粒质量以实现高效生产(与图 1 相关)。
A-B. 在 150mm 培养皿中生产 SARS2 Luc VLPs,包括 4P VLPs(图 A)和 3P VLPs(图 B),所有情况下保持总质粒质量恒定在 50 µg/皿,同时改变刺突蛋白质粒的比例(0-4 µg)。通过测量受体293T-hACE2 细胞中的发光来评估 VLP 进入特性。两种系统均在使用 1 µg 刺突蛋白质粒时达到最高进入效率。
C. 动态光散射(DLS)定量了 3P SARS2 Luc-PS9 VLPs 的颗粒尺寸分布。带有刺突蛋白的 VLPs 尺寸约为 146 nm,略大于无刺突蛋白的 VLPs(约 125 nm)。
D. 图 1G(主图)中数据的代表性流式细胞术直方图。在这些测量 3P SARS2 EGFP-PS9 VLP 进入 293T-hACE2 或 A549-hACE2-TMPRSS2 细胞的研究中,观察到绝大多数细胞有明显的EGFP 表达。
图2:通过更换病毒糖蛋白(VSV-G、SARS2、SARS、MERS)调控VLP的细胞趋向性,实现特异性细胞感染。
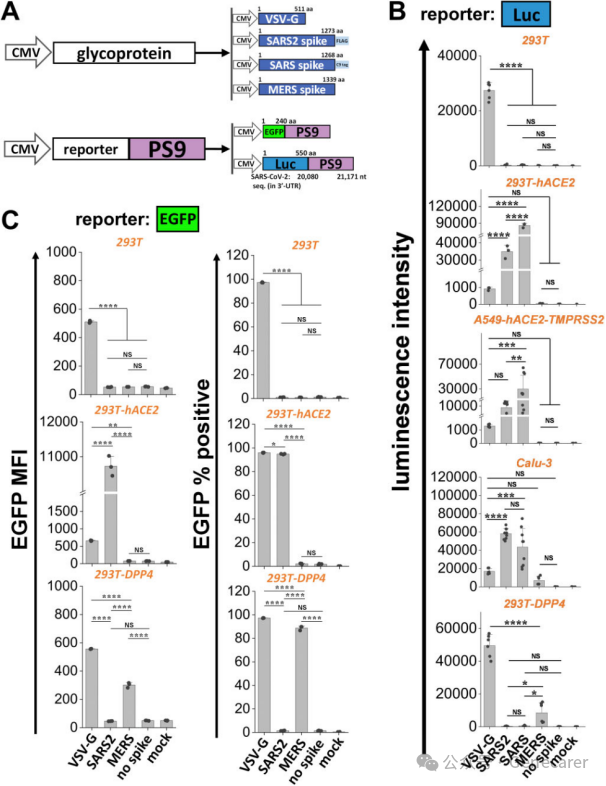
(A) 使用3P系统,通过改变病毒糖蛋白(VSV-G、SARS2刺突蛋白、SARS刺突蛋白或MERS刺突蛋白)和报告基因(荧光素酶或EGFP),制备了不同类型的VLPs。
(B) 使用1微克病毒糖蛋白制备了各种3P Luc-PS9 VLPs,并用它们感染五种细胞类型:野生型293T (293T)、293T-hACE2、A549-hACE2-TMPRSS2、Calu-3和293T-DPP4。SARS2和SARS刺突蛋白VLPs表现出相似的趋向性,仅进入表达hACE2的细胞(293T-hACE2、A549-hACE2-TMPRSS2和Calu-3),且SARS的发光强度高于SARS2。MERS VLPs以较低水平感染Calu-3细胞,并能有效进入293T-DPP4细胞。VSV-G VLPs可进入所有细胞类型。
(C) 使用4 μg VSV-G、1 μg SARS2刺突蛋白或1 μg MERS刺突蛋白质粒制备了3P EGFP-PS9 VLPs。VSV-G VLPs可进入所有细胞类型。SARS2 VLPs仅进入ACE2细胞。MERS VLPs仅进入DPP4细胞。方法部分提供了VLP生产的详细步骤。
图S2. 调控病毒趋向性(与图2相关)。
A. 建立了稳定的同源293T-DPP4细胞系,并使用Alexa Fluor 488标记的抗DPP4抗体通过流式细胞术检测了DPP4的表达水平。
B. 图2B(主图)中展示的VLP进入数据也是在提高发光检测板阅读器的检测灵敏度下收集的。数据显示,VSV-G VLP具有很强的进入效率,尽管对于293T-hACE2和A549-hACE2-TMPRSS2细胞,其效率低于SARS2或SARS VLP。
C-D. 在150mm培养皿中生产带有VSV-G(C)和MERS(D)刺突蛋白的3P Luc-PS9 VLP时,改变了相应糖蛋白质粒的用量。使用4 µg VSV-G或2 µg MERS刺突蛋白质量生产的VLP能引起靶细胞的最大感染。
E. 图2C(主图)的代表性流式细胞术直方图,显示可以通过改变病毒糖蛋白来改变VLP的趋向性。
图3:开发双质粒(2P)系统,简化VLP制备流程,部分构建体(如2P.2)表现出与4P相当的感染效率。
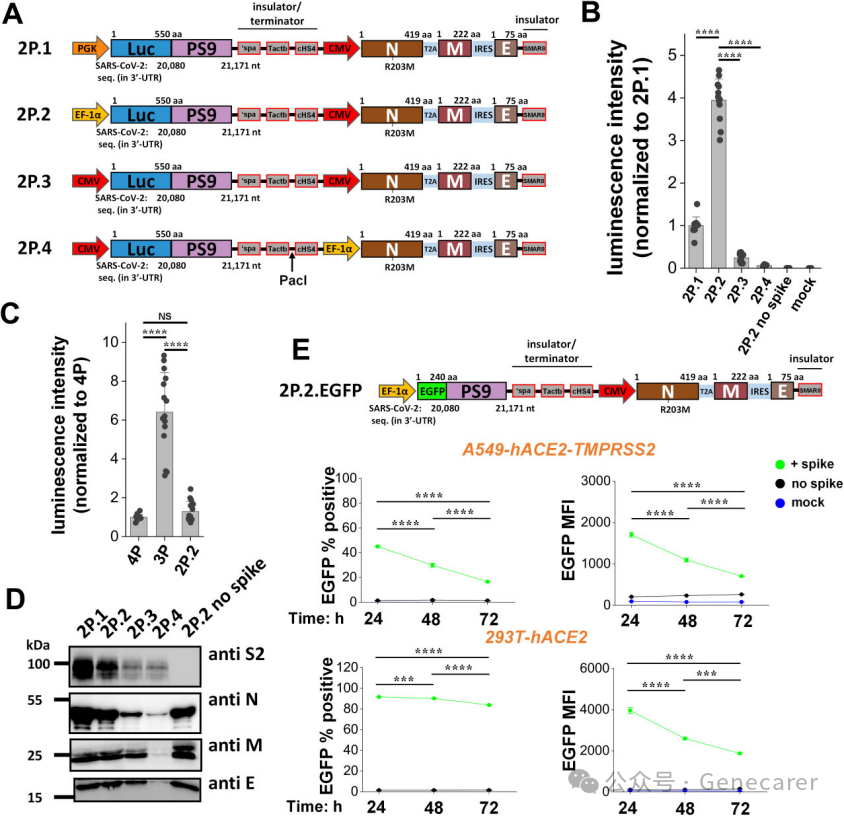
采用双启动子系统优化VLP技术。
(A)开发了四种构建体,其中两个独立启动子分别驱动报告基因和SARS2结构蛋白的表达。启动子间通过绝缘子和终止子序列隔离以减少启动子干扰:合成polyA(spa);β-肌动蛋白来源的G富集序列(Tactb);鸡超敏位点4(cHS4);以及E蛋白末端的合成MAR序列8(sMAR8)。
(B,C)将每种构建体与刺突蛋白质粒共转染293T细胞,制备四种不同的2P SARS2 Luc-PS9 VLP。2P.2 VLP显示出最高的荧光强度(B),其信号与4P VLP相当但低于3P VLP(C)。
(D)SARS2结构蛋白的Western blot结果显示不同2P质粒的蛋白表达模式存在差异。2P.2 SARS2 Luc-PS9 VLP的蛋白条带强度高于2P.3和2P.4,但低于2P.1。(E)通过将荧光素酶报告基因替换为EGFP构建2P.2.EGFP VLP。流式细胞术检测显示2P.2.EGFP SARS2 VLP可有效进入A549-hACE2-TMPRSS2和293T-hACE2细胞。
图4:展示3P VLPs可包装最多四个报告基因(EGFP、dTomato、TagBFP、Luc),但随着mRNA长度增加,报告信号逐渐减弱。
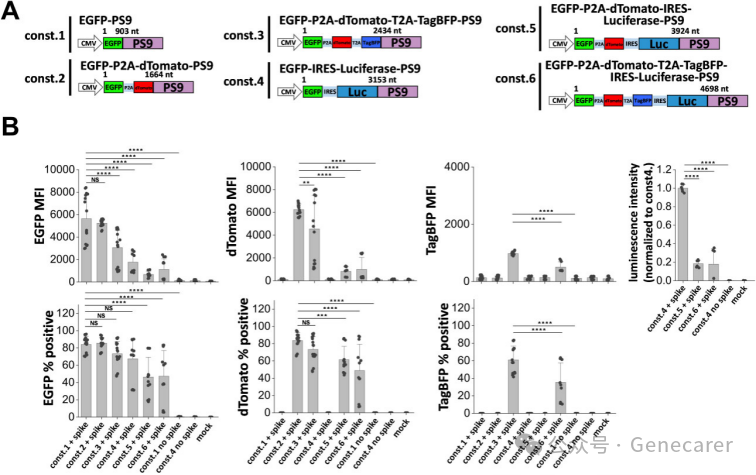
使用3P SARS2 VLP递送四种转基因。
(A)六种PS9构建体的示意图,其中依次添加了四种不同的报告基因:EGFP、dTomato、TagBFP和/或荧光素酶。这些构建体被用于开发递送转基因的3P VLP。(B)使用不同3P构建体(各样本中VLP用量相同)进行多次生物学重复的荧光及发光信号检测。根据报告基因强度(上图)和荧光阳性细胞百分比(下图)评估了载荷大小与病毒侵入效率的关系。随着包装mRNA长度的增加,被感染细胞百分比呈逐步下降趋势,而荧光强度的下降幅度更为显著。
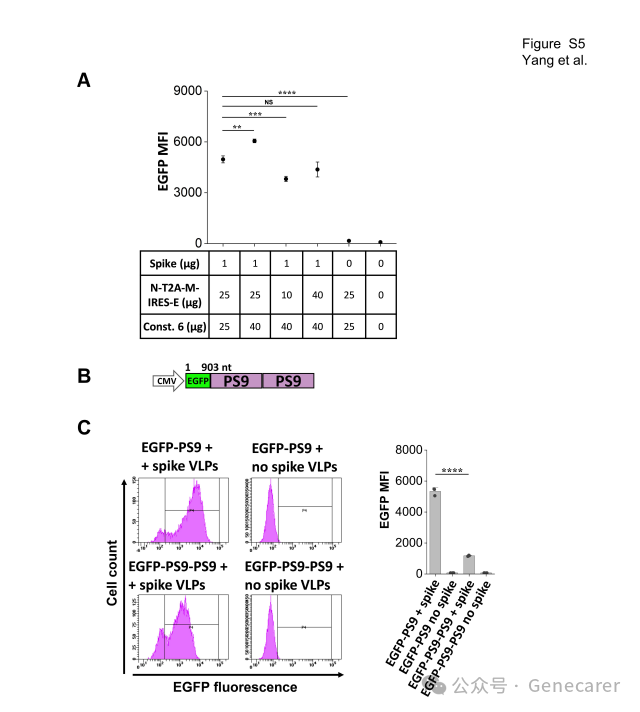
图S5. 提升 VLP 功效的策略(与图 4 相关)。
A. 在 VLP 生产过程中改变质粒用量,以确定生成 3P VLP 所需的最佳化学计量比。这些研究使用 const. 6 作为有效载荷。图中列出了每种情况下刺突蛋白质粒、N-T2A-M-IRES-E 质粒和 const. 6 质粒的用量。与使用等量 N-T2A-M-IRES-E 和 const. 6 质粒(均为 25 µg)的标准化学计量比相比,将 const. 6 质粒用量增加至 40 µg 可使病毒进入效率提高约 25%。测试的其他条件均降低了 EGFP 信号。
B. 在原始 PS9 包装信号的末端附加了一个重复的 PS9 包装信号,从而构建了 EGFP-PS9-PS9。
C. 对于 3P VLP 系统,基于荧光强度测量,该构建体未能增强病毒进入效率。
图5:分析不同大小mRNA对VLP组装和功能的影响,发现mRNA长度不影响VLP物理组装,但影响目标细胞中的蛋白表达。
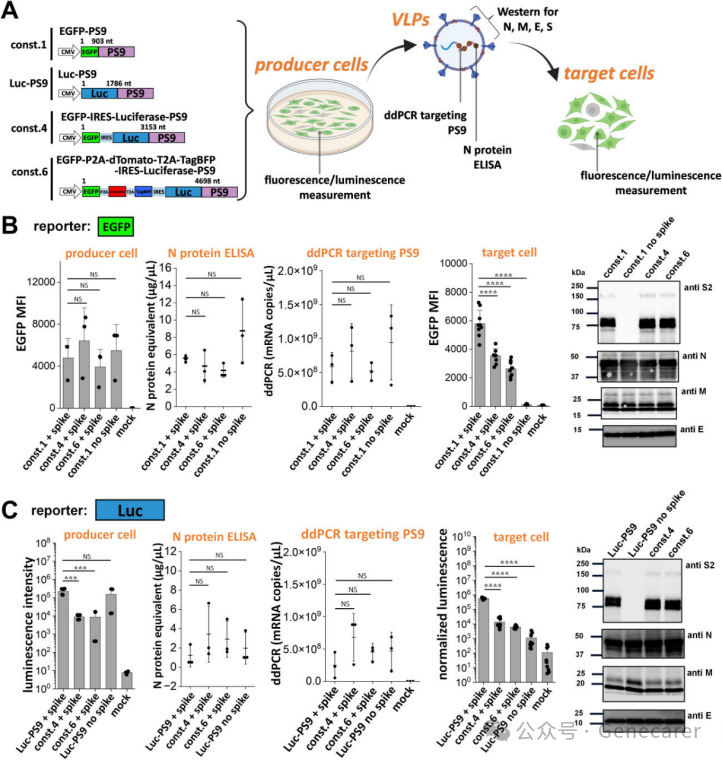
调控VLP功能与效力的机制。
(A)采用3P系统分别制备了携带CMV启动子下游EGFP报告基因、以及携带CMV或IRES启动子下游荧光素酶报告基因的VLPs,并检测了图示各项参数。(B, C) 这些图表中从左至右的单个面板分别展示:
数据显示:所有负载类型的VLP均产生了结构组成与mRNA拷贝数相似的病毒样颗粒,但增大负载尺寸会渐进性降低靶细胞中的报告信号。
图6:使用携带Cas9 mRNA的VLPs进行基因编辑,成功敲除EGFP、hACE2和SLC35A1基因,编辑效率达20%–85%。
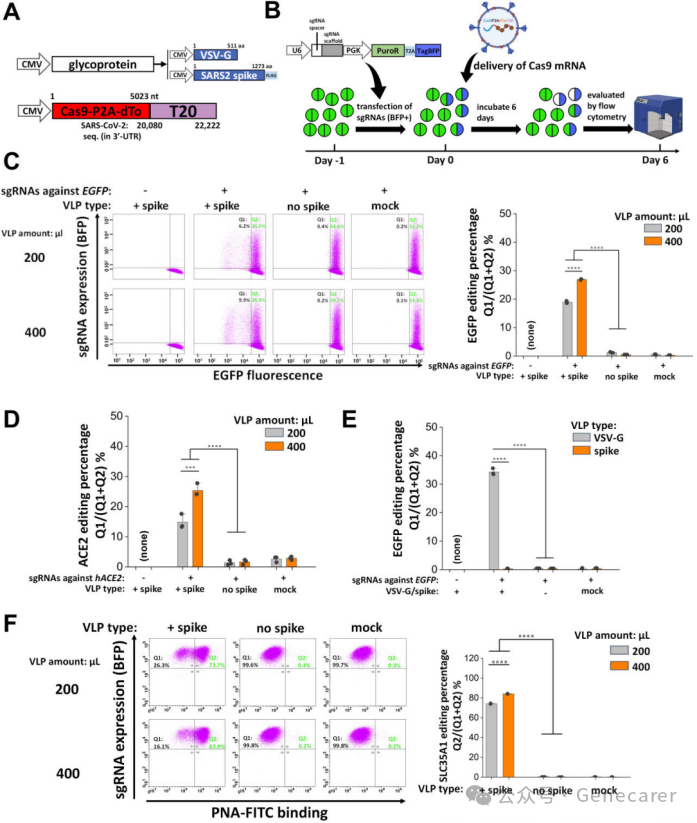
VLP向靶细胞递送功能性Cas9 mRNA实现基因编辑。
(A)采用表面糖蛋白为VSV-G或SARS2刺突的3P Cas9-P2A-dTo-T20 VLP(dTo:dTomato红色荧光蛋白)进行基因编辑研究。
(B)(C)-(E)面板中基因编辑研究的工作流程示意图:在-1天通过携带BFP报告基因的质粒将sgRNA转染至细胞;第0天通过VLP递送spCas9 mRNA;VLP趋向性取决于表面糖蛋白类型;第6天定量基因编辑效率。编辑效率通过BFP阳性群体中EGFP表达缺失(面板C和E)或基于抗hACE2结合检测的ACE2表达缺失(面板D)的百分比进行量化。
(C)在293T-hACE2-EGFP细胞中导入靶向EGFP的sgRNA,并通过3P SARS2 Cas9-P2A-dTo-T20 VLP递送spCas9 mRNA。
(D)在293T-hACE2细胞中通过3P SARS2 Cas9-P2A-dTo-T20 VLP导入靶向hACE2的sgRNA以敲除该受体。
(E)在293T-EGFP细胞中导入靶向EGFP的sgRNA,分别使用携带VSV-G或SARS2刺突的3P Cas9-P2A-dTo-T20 VLP进行基因组编辑。所有实验均显示,在表达sgRNA的细胞中实现了20%-35%的靶基因(EGFP或hACE2)敲除效率,且较高VLP用量可提升编辑效果。
(F) 用3P SARS2 Cas9-P2A-dTo-T20 VLP(1.885 μg/μl N蛋白当量)或无SARS2刺突的VLP(1.385 μg/μl N蛋白当量)感染稳定表达靶向SLC35A1的sgRNA的293T-hACE2细胞。通过荧光花生凝集素(PNA)与细胞结合的增加评估基因编辑效率,使用3P VLP编辑内源基因时观察到超过70%的编辑效率。各实验所用VLP体积详见对应面板标注。数据以均值±标准差表示。*P < 0.001,**P < 0.0001,NS:无统计学意义。
图7:在小鼠模型中证实VLPs可通过滴鼻或口咽灌注途径递送mRNA至肺部,VSV-G VLPs效率高于maSARS2 VLPs。
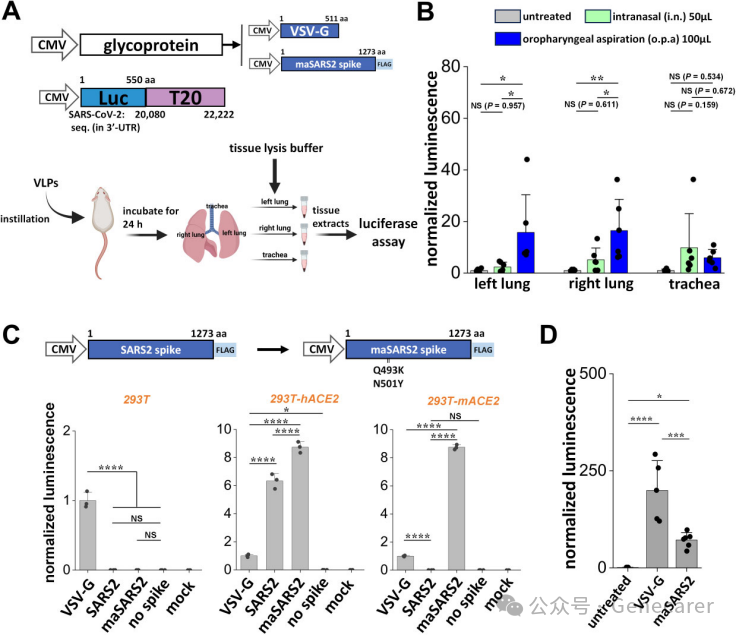
使用VLP进行体内肺部基因递送。
(A)携带VSV-G或maSARS2的VLP在时间=0时滴注至小鼠体内。滴注后二十四小时,在左肺、右肺或气管的组织提取物中测量荧光素酶活性。采用裂解液中的蛋白质浓度对发光信号进行标准化,所有体内研究中未处理/模拟组的数值均设为1.0。
(B)通过口咽灌注(100μl)或鼻内灌注(50μl)途径滴注VSV-G VLP。口咽灌注使VLP递送至小鼠肺部。
(C)将Q493K和N501Y突变引入SARS2刺突蛋白以生成maSARS2刺突蛋白。分别制备了带有VSV-G、SARS2、maSARS2及无刺突蛋白的3P VLP,其N蛋白当量浓度分别为1.859、1.149、1.334和2.024 μg/μl。使用50μl VLP感染三种靶细胞:293T、293T-hACE2和293T-mACE2。VSV-G VLP可感染所有三种细胞类型,SARS2刺突仅感染293T-hACE2(人ACE2),而maSARS2刺突对293T-hACE2和293T-mACE2均具有感染性。本组实验中VSV-G的发光信号值设为1.0。
(D) 通过口咽灌注将100微升VSV-G VLP或maSARS2 VLP(N蛋白当量浓度均为0.820 μg/μl)滴注至小鼠体内。采集全肺组织。未接受VLP处理的小鼠作为阴性对照。VSV-G和maSARS2 VLP均能在小鼠肺部产生荧光素酶信号,其中VSV-G效率更高。
二、文章用的质粒组合
4P系统:M-IRES-E、N、Luc-PS9、Spike
3P系统:N-T2A-M-IRES-E、Luc-PS9、Spike
2P系统:LVDP系列(如2P.1–2P.4) + Spike
其他质粒:VSV-G(pMD2.G)、MERS Spike、SARS Spike、Cas9-P2A-dTomato-PS9/T20等
三、包装方法
1 使用293T细胞作为生产细胞。
2 通过钙磷酸法或Lipofectamine 2000转染质粒。
3 转染后6–8小时更换为Opti-MEM培养基。
4 48小时后收集上清,离心去除细胞碎片。
5 超速离心(150,000 × g,2.5小时)浓缩VLPs。
6 重悬VLPs于PBS中,-80°C保存。
四、结果与讨论
1、简化系统:3P和2P系统简化了VLP生产流程,提高了效率与一致性。
2、趋向性调控:通过更换糖蛋白实现细胞特异性感染。
3、包装能力:VLPs可包装长达5 kb的mRNA,最多四个转基因。
4、基因编辑:成功递送Cas9 mRNA实现高效、细胞特异性基因编辑。
5、体内递送:VLPs可克服肺部生理屏障,实现mRNA靶向递送递送。
