杆状病毒载体创新应用,首次在哺乳动物原代肌肉干细胞中实现大型机械敏感离子通道PIEZO1的高效表达与功能研究。
在原代干细胞中进行大型基因的功能研究一直是技术难点。近期,一项研究通过改良杆状病毒载体系统,成功建立了在肌肉卫星细胞中高效表达大型基因PIEZO1的方法。这项技术不仅克服了传统转染方法的限制,也为研究其他大型蛋白在干细胞中的功能提供了可靠平台。
01大型基因在原代细胞中的转导挑战
在肌肉生物学研究中,许多关键蛋白由大型基因编码,如机械敏感离子通道PIEZO1(约77kb)。传统脂质体转染方法在将这类大型基因导入细胞时效率有限。
研究团队首先尝试在C2C12成肌细胞系中使用脂质体转染PIEZO1-EGFP融合基因,但流式细胞术分析显示,其荧光信号与未转染对照组无显著差异。相比之下,转染单一EGFP报告基因的对照组则表现出明显的荧光增强。
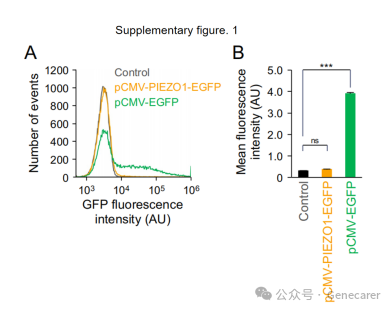
补充图1.使用脂质体转染试剂将编码PIEZO1-EGFP的质粒转染到C2C12细胞中的低转染效率。
(A) 使用Lipofectamine 2000转染pCMV-EGFP质粒(绿色)或pCMV-PIEZO1-EGFP质粒(黄色)的C2C12细胞中GFP荧光强度的流式细胞术分析。(B) 流式细胞术分析的细胞平均荧光强度。N=3,n=30,000个细胞,平均值 + 标准误,***p < 0.001;n.s.,不显著。
这一结果突显了大型基因转导的技术瓶颈,也解释了为何需要开发新的基因递送方法。
02杆状病毒载体系统的优化与应用
为解决大型基因转导难题,研究团队采用了杆状病毒载体系统。该系统具有高达38kb的包装容量,远高于常用的慢病毒等载体。
研究人员使用一种经过改良的杆状病毒表达系统,该系统在水泡性口炎病毒G蛋白的作用下能够有效感染哺乳动物细胞。该团队构建了携带PIEZO1-EGFP融合基因的重组杆状病毒载体,并成功在昆虫细胞中生产出高滴度的病毒颗粒。
通过逐步优化感染条件,研究人员发现了一个关键转折点:当在27°C环境下使用PBS缓冲液进行病毒感染时,转导效率显著提高。
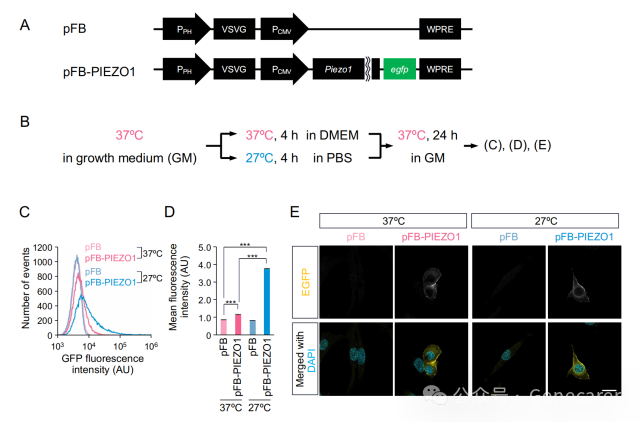
图1.在C2C12细胞中杆状病毒介导的PIEZO1-EGFP表达。
(A)显示表达PIEZO1-EGFP(pFB-PIEZO1)的重组供体质粒的示意图。缺乏PIEZO1-EGFP序列的质粒(pFB)用作对照。PH;多角体蛋白,VSVG;水泡性口炎病毒G蛋白,WPRE;土拨鼠肝炎病毒转录后调控元件。(B) 杆状病毒介导基因转移到C2C12细胞的概述。(C) C2C12细胞中GFP荧光强度的流式细胞术分析(30,000个细胞)。(D) 流式细胞术分析的细胞平均荧光强度。N=3,平均值 + 标准误,***p < 0.001。(E) C2C12细胞中表达的PIEZO1的免疫荧光染色。使用抗GFP抗体(黄色)检测PIEZO1-EGFP。DAPI(蓝色)指示细胞核。比例尺:20 µm。
补充图3.温度和培养基pH对病毒转导的影响。
(A) 在所示培养条件下杆状病毒转导到C2C12细胞中。(B) PIEZO1蛋白表达的免疫印迹分析。在所示培养条件下用重组杆状病毒转导C2C12细胞。使用抗GFP抗体和抗α-微管蛋白抗体分别检测PIEZO1和α-微管蛋白的量。α-微管蛋白用作上样对照。
研究人员表示:“降低温度可能改变了病毒内吞或内体逃逸的动力学过程。这为我们提供了一种简单却高效的优化策略。”优化后的条件使杆状病毒系统成功克服了大型基因的递送障碍,为后续在原代细胞中的应用奠定了基础。
03外源表达蛋白的结构与功能验证
成功转导后,研究团队对外源表达的PIEZO1蛋白进行了全面表征。免疫印迹分析显示,在感染细胞中可检测到分子量约300kDa的全长PIEZO1-EGFP融合蛋白。
亚细胞定位分析表明,PIEZO1-EGFP主要定位于细胞质膜,这与内源性PIEZO1的分布一致。钙成像实验进一步证实,在PIEZO1缺陷细胞中,通过杆状病毒导入的PIEZO1能够介导Yoda1诱导的钙离子内流,恢复了离子通道功能。
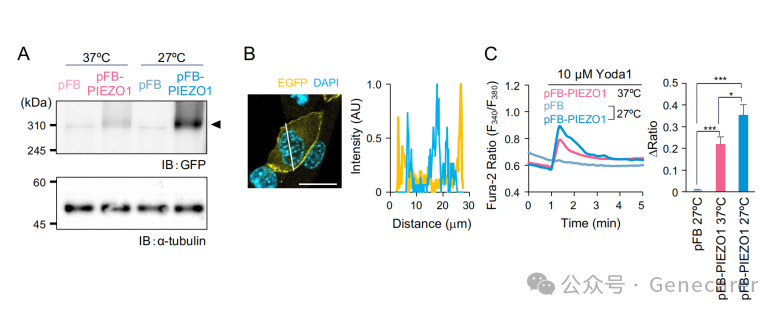
图2.使用杆状病毒系统在C2C12细胞中表达的PIEZO1-EGFP作为离子通道的功能表征。
(A) PIEZO1-EGFP蛋白表达免疫印迹分析的代表性图像。从用重组杆状病毒感染的C2C12细胞制备裂解液后,分别使用抗GFP抗体和抗α-微管蛋白抗体检测对应于PIEZO1和α-微管蛋白的蛋白条带。α-微管蛋白用作上样对照。(B) 用重组杆状病毒转导的C2C12细胞中PIEZO1-EGFP的荧光强度谱。沿白线的强度谱显示在左图。使用抗GFP抗体(黄色)检测PIEZO1-EGFP。DAPI(蓝色)指示细胞核。比例尺:20 µm。(C) 在所示条件下用重组杆状病毒转导的_Piezo1_缺陷型C2C12细胞中Yoda1诱导的Ca²⁺动员的Fura-2比率测量(F340/F380)(左)。Fura-2比率的变化(Δ比值)在右图中量化。n=99,平均值 + 标准误,p < 0.05,**p < 0.001。
为测试离子通道的功能完整性,研究者在PIEZO1缺陷的细胞系中进行了钙成像实验。当使用特异性激动剂Yoda1刺激时,只有通过杆状病毒导入了PIEZO1的细胞表现出明显的钙离子内流。这说明外源表达的PIEZO1不仅结构完整,而且保持了作为机械敏感离子通道的活性。钙信号响应的恢复是功能验证的重要一步。这些结果表明,杆状病毒系统不仅能实现大型基因的递送,还能保证表达蛋白的正确折叠和功能完整性。
04在原代肌肉干细胞中的高效转导
研究团队进一步将该方法应用于从小鼠骨骼肌分离的原代肌肉卫星细胞。这些细胞在不同培养阶段具有不同的状态:分离初期多为静止状态,24小时后进入激活状态,随后可能向肌源性分化。
实验结果显示,杆状病毒在激活状态的MuSCs(分离后24小时)中转导效率最高,达到约74%。即使在静止期细胞中,转导效率也有24%,显著高于许多传统方法在静止干细胞中的表现。
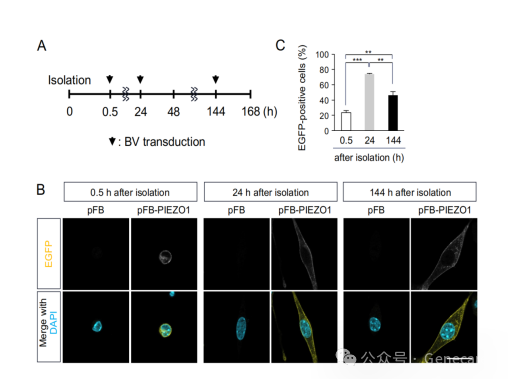
图3.在小鼠分离的肌肉卫星细胞中杆状病毒介导的PIEZO1-EGFP表达。
(A)显示杆状病毒转导到小鼠肢体肌肉分离的MuSCs中的示意图。(B) 分离MuSCs中PIEZO1-EGFP表达的荧光免疫染色分析。分别在分离后0.5、24和144小时用重组杆状病毒转导MuSCs,分别代表静止MuSCs、激活MuSCs和分化成肌细胞。使用抗GFP抗体(黄色)检测PIEZO1。DAPI(蓝色)指示细胞核。比例尺:30 µm。(C) 分离后0.5、24和144小时用重组杆状病毒转导的PIEZO1表达细胞的百分比。N=3,平均值 + 标准误,n > 100,p < 0.01,*p < 0.001。
补充图4.杆状病毒转导前分离MuSCs激活/分化状态的评估。
分离后指定时间点肌肉卫星细胞中MYOD(红色)和PAX7(绿色)的免疫荧光分析(A)。量化表达MYOD和/或PAX7的细胞的百分比(B)。DAPI(蓝色)指示细胞核。比例尺:100 µm。N=3,n > 200个细胞,平均值 + 标准误,p < 0.05,p < 0.01,p < 0.001。
即使在分离后立即处于静止状态的肌肉干细胞中,转导效率也达到了24%,这在静止干细胞基因转导中是一个显著的成绩。相比之下,传统的病毒载体在静止干细胞中的转导效率通常很低。
杆状病毒表达的PIEZO1在肌肉干细胞中同样表现出正确的膜定位和功能活性,这表明该系统能够有效克服大型基因在原代细胞中表达的障碍。这一发现对于研究MuSCs在肌肉再生中的功能具有重要意义,因为激活状态是MuSCs发挥修复功能的关键阶段。
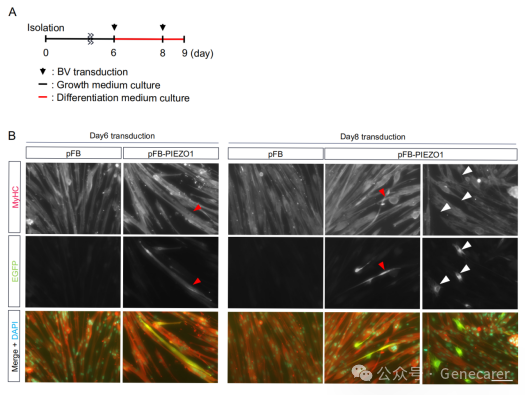
图4.在分化肌肉卫星细胞中杆状病毒介导的PIEZO1表达。
(A) 分离MuSCs分化和杆状病毒介导基因转移的时间进程。(B) 在分化诱导前(第6天)或后(第8天)用重组杆状病毒转导的分化MuSCs中PIEZO1的免疫荧光染色。蓝色、绿色和红色分别代表细胞核、PIEZO1和MyHC。红色箭头:MyHC和EGFP阳性细胞,白色箭头:MyHC阴性和EGFP阳性细胞。比例尺:100 µm。
图5.使用杆状病毒系统在分离MuSCs中表达的PIEZO1-EGFP作为离子通道的功能表征。
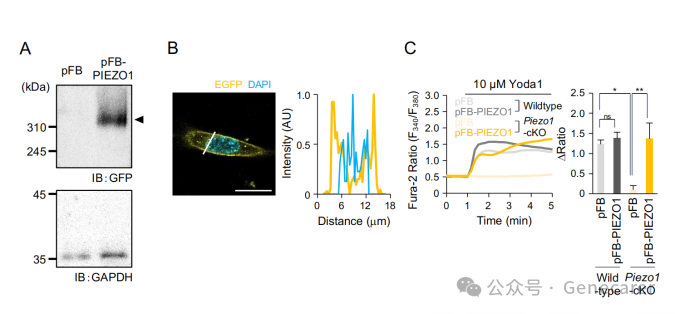
(A) PIEZO1蛋白表达的免疫印迹分析。分离后24小时用重组杆状病毒转导分离的MuSCs。分别使用抗GFP抗体和抗GAPDH抗体检测PIEZO1和GAPDH。GAPDH用作上样对照。(B) 用重组杆状病毒转导的分离MuSCs中PIEZO1-EGFP的荧光强度谱。沿白线的强度谱显示在上图。使用抗GFP抗体(黄色)检测PIEZO1-GFP。DAPI(蓝色)指示细胞核。比例尺:20µm。(C) 用重组杆状病毒转导的MuSCs中Yoda1诱导的Ca²⁺内流的Fura-2比率测量(F340/F380)(左)。MuSCs从野生型(WT,N=4)或MuSC特异性_Piezo1_缺陷(Piezo1-cKO,N=3)小鼠分离,每次分析99个细胞。Fura-2比率的变化(Δ比值)在右图中量化。平均值 + 标准误,*p < 0.05,**p < 0.01;n.s.,不显著。
05恢复基因缺陷细胞的生理功能
为验证该方法在功能研究中的应用价值,研究团队在PIEZO1条件性敲除的MuSCs中进行了功能回补实验。
EdU掺入实验表明,PIEZO1缺失导致MuSCs增殖能力下降。通过杆状病毒重新导入PIEZO1基因后,细胞的增殖能力恢复到与野生型相当的水平。
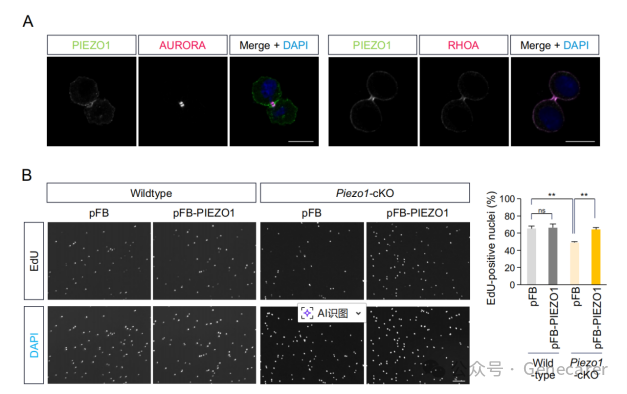
图6.在增殖MuSCs中对杆状病毒表达的PIEZO1-EGFP的功能评估。
(A)细胞分裂期间PIEZO1-EGFP定位的荧光免疫染色分析。分离后24小时用重组杆状病毒转导分离的MuSCs。使用特异性抗体检测AURORA和RHOA作为细胞分裂成分。比例尺:10 µm。(B) 分离后24小时用重组杆状病毒转导的MuSCs中5-乙炔基-20-脱氧尿苷(EdU)掺入试验的荧光图像(左)。MuSCs从野生型(WT,N=3)或MuSC特异性_Piezo1_缺陷(Piezo1-cKO,N=5)小鼠分离,每次分析> 400个DAPI阳性细胞。EdU和DAPI阳性细胞的百分比在右图中量化。DNA生物合成速率通过测量分离后72小时的EdU掺入来评估。比例尺:100 µm。平均值 + 标准误,**p < 0.01;n.s.,不显著。
特别值得注意的是,杆状病毒导入的PIEZO1在细胞分裂过程中能够正确定位到中间体,并与细胞分裂相关蛋白AURORA激酶和RHOA共定位。这表明外源表达的PIEZO1在细胞分裂这一精细过程中也具有功能意义。
该研究团队还尝试在由肌肉干细胞分化而来的肌管中表达PIEZO1。研究者发现,若在肌管形成前进行病毒感染,PIEZO1可以在终末分化的肌管中成功表达;若在肌管形成后再感染,表达效率则大幅降低。
总结与展望
本研究成功建立了一种基于杆状病毒载体的大型基因转导方法,首次在哺乳动物原代肌肉卫星细胞中实现了PIEZO1的高效表达和功能研究。该方法具有以下优势:
高包装容量:可递送大小超过77kb的大型基因
高效转导:在激活态MuSCs中效率达74%,在静止细胞中也有一定效率
功能完整:表达蛋白具有正确的亚细胞定位和离子通道活性
应用广泛:可用于基因功能研究、信号通路解析和疾病模型构建
该技术平台不仅为PIEZO1在肌肉生物学中的功能研究提供了有力工具,也为研究其他大型蛋白在组织干细胞中的作用开辟了新途径。未来,通过进一步优化载体设计和转导条件,这一方法有望应用于更多类型的原代细胞和干细胞,推动组织再生和疾病治疗研究的发展。
