稳转细胞系即稳定表达细胞系,即目标基因表达元件(过表达元件、干扰shRNA元件)整合在宿主基因的基因组中,随着细胞传代可以稳定表达,稳转细胞系构建主要有几种方案:
一、慢病毒感染细胞稳转细胞系构建:
慢病毒因为可以感染大多数的分裂细胞和非分裂细胞,包装技术成熟,II代和III代慢病毒包装系统均能包装高滴度的慢病毒,是稳转细胞系构建的首选系统。但是因为慢病毒有包装容量限制,不适合转录本区域比较长的基因,对较大的基因有局限性。另外由于慢病毒是逆转录病毒,病毒表达载体中,是由WPRE元件代替PolyA稳定以达到稳定mRNA的作用,对部分基因的翻译有一定影响。
二、转座子介导的稳转细胞系构建:
转座子(Transposon)也称“跳跃基因”,由美国科学家芭拉拉·麦克林托克在研究玉米颗粒颜色时发现。是普遍存在于各种生命细胞内的可移动的遗传信息元件,通过“剪切和粘贴”机制实现DNA片段在染色体内部/之间高效转移。 工程化的转座子是由两部分组成,包括位于转座子基因两侧的顺式元件短末端反向重复序列(ITR)和位于两个ITR序列之间的转座酶编码基因序列。转座子是通过编码转座酶,转座酶与ITR序列结合介导转座酶基因在基因序列之间的转移。将转座子的两个元件分离并构建在两个独立在载体上,原来转座酶的序列替换成感兴趣的基因序列(GOI),而转座酶在另外一个载体上独立表达,将两个载体共转染目的细胞,就能实现目的基因在宿主基因组上整合,与其他技术的不同(慢病毒载体介导的基因组整合),在整合酶存在的情况,目的基因会一直处于切割—整合的状态,即连续在基因组上跳跃。
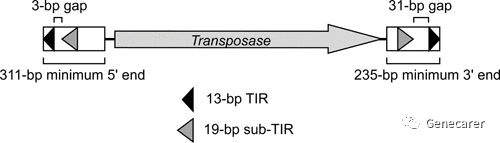
转座子稳转细胞系主要的优势是其对基因大小没有严苛的限制,文章报道最多可以实现200kb的基因插入,另外,随着睡美人转座系统的不断优化,转座子插入效率提高了100倍以上,整合效率与慢病毒效率相当。缺点是因为转座子系统为了达到更好的整合效率,一个目的基因的拷贝大约需要4个睡美人转座子SB100x转座酶,所以转座酶和目的基因是单独的骨架载体,依赖于细胞的质粒转染效率,对于原代细胞、难转染的细胞等有一定限制。随着SB100X转座酶I212S和C176S两个突变位点的改进。改变了转座酶的稳定性,溶解性,显著降低了转座酶被纯化为具有活性重组蛋白的的技术难度。通过引入这两个突变,创建了一种新型的转座酶突变体,可以通过RNP的方式将转座酶和目的基因表达载体电转细胞,实现高效率的整合。但是通过转座子RNP的方式进行稳转株的构建,对设备提出了更高的要求。
三、CRISPR/Cas9 基因敲入稳住细胞系构建:
采用CRISPR/Cas9系统进行目的基因(外源基因,抗性基因和荧光标志等)的定点敲入,是通过提供外源模板(Donor载体)依靠细胞自身的修复机制NHEJ(非同源末端连接)和HDR(同源同组)完成的。在哺乳动物细胞中,CRISPR/Cas9介导的NHEJ对标记基因的插入概率明显高于HDR修复机制。
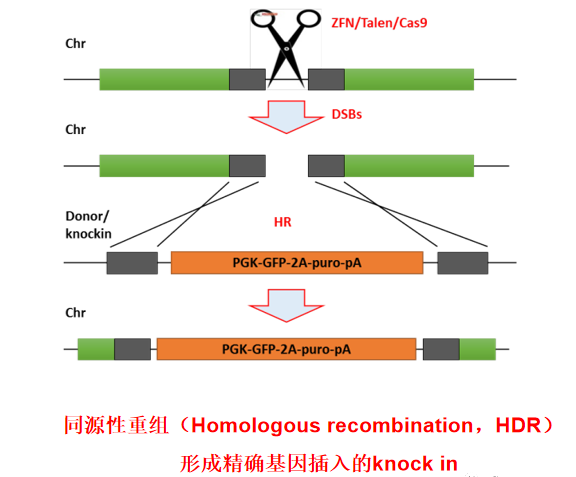
利用CRISPR/Cas9基因敲入构建稳转细胞系,通过设计人PPP1R12C基因的第一个内含子上(AAVS1位点,人基因组安全港)位点sgRNA和donor载体,利用不同的递送系统递送目的细胞,实现gRNA位置的基因定点敲入。在该位点中插入外源基因片段具有稳定表达、不影响其他基因转录的优点。相对于慢病毒和转座子系统,基因敲入方法是基因定点插入,细胞基因型一定,不存在随机插入的风险。但基因敲入的概率不同细胞,不同位点差异较大,并且需要挑取单克隆以得到基因型一定的稳转细胞克隆株。随着基因编辑效率的不断提高,利用AAVS1位点基因敲入构建稳转细胞系会越来越省时省力。
四、CRISPR SAM系统,通过融合VP64、MS2-P65-HSF1系统进行稳转细胞系构建:
CRISPR SAM通过dCas9-VP64融合蛋白、MS2-P65-HSF1结合激活蛋白三个原件,实现了对多数细胞内源基因的特异性激活。CRISPR SAM主要优势是不受基因大小限制,但需要三种不同抗性病毒逐次或同时感染目的细胞,
CRISPR SAM常用载体 | 表达元件 | 元件作用 | 抗性 |
lenti dCAS-VP64_Blast | dCas9+VP64 | dCas9蛋白融合转录激活因子VP64 | Blast |
lenti sgRNA(MS2)_zeo | sgRNA+MS2 loop | gRNA结合在TSS上游 | zeo |
lenti MS2-P65-HSF1_Hygro | MS2-N55K,p65,HSF1 | 转录激活级联放大 | Hygro |
表1 CRISPR SAM常用载体元件
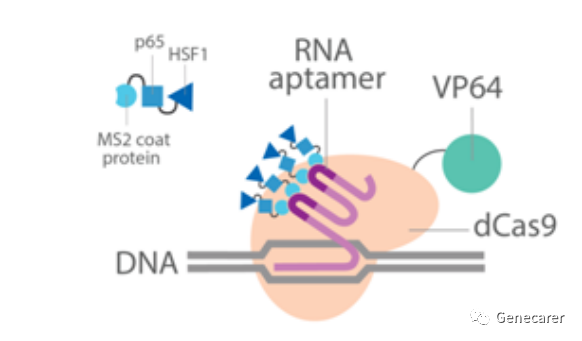
CRISPR SAM主要将sgRNA序列构建在lenti sgRNA(MS2)_zeo载体中,配合另外两种慢病毒即可实现任何一个基因的特异性激活,为基因功能研究尤其表观遗传文库筛选提供了更广阔的应用前景。主要缺点是需要三种不同抗性的病毒对细胞进行筛选,部分细胞经三种抗性筛选后表型变化明显。
根据不同的基因,不同的细胞选择不同的构建方法是稳转细胞系构建的第一步,也是最重要一步,根据项目经验和理论判断,总结如下规律,可做参考:
判断指标 | 慢病毒稳转细胞系 | 转座子稳转细胞系 | CRISPR/Cas9基因敲入稳转细胞系 | CRISPR SAM稳转细胞系构建 |
基因大小 | 0-4kb | 3.5kb-7.5kb | 0-5.5kb | ≥7.5kb |
蛋白种类 | 可溶性蛋白 | 可溶性蛋白,膜蛋白 | 可溶性蛋白,膜蛋白 | 可溶性蛋白,膜蛋白 |
细胞种类 | 分裂细胞和非分裂细胞 | 易转染细胞 | 易转染/易电转细胞 | 抗生素不敏感细胞 |