
北海道大学药学院创新纳米医学实验室开发了一种新型脂质组合,该组合可以有效且高度选择性地将质粒DNA (pDNA)递送至脾脏中的免疫细胞。使用DODAP(一种以前被认为对于基因传递效率低下的可电离脂质),首次证明,这种被忽视的脂质可以成功地用于体内高效和靶向基因传递,当与DOPE组合(一种特定的辅助脂质;使用一定的DODAP和DOPE比例可形成脂质纳米颗粒(LNP),其基因表达量提高约1000倍,并且这种表达对脾脏具有特异性,使其成为使用pDNA转染时最具脾脏选择性的系统。开发的DODAP/DOPE-LNP通过补体C3 受体靶向脾脏中的免疫细胞,该途径对于有效的基因表达至关重要。作者推测 DODAP/DOPE-LNP的高脾脏转染活性是通过补体受体促进与B细胞激活相关的基因表达引起的。包封肿瘤抗原编码pDNA的LNP显示出预防性和治疗性抗肿瘤作用。优化后的LNP可产生不同的细胞因子和抗原特异性抗体,并发挥抗原特异性细胞毒作用。这项研究复兴了 DODAP在基因递送中的应用,并强调了使用适当的脂质组合将基因递送至特定细胞的重要性。
而脂质纳米颗粒 (LNP) 是将治疗性核酸(例如短干扰RNA (siRNA)、信使RNA (mRNA) 和质粒DNA (pDNA))递送至患病组织和细胞内作用位点的先进技术之一。用于体内基因递送的有效LNP由可电离的阳离子脂质、磷脂、胆固醇 (Chol) 和聚乙二醇 (PEG) 脂质组成。当使用基于脂质的载体时,可电离的阳离子脂质是有效核酸递送的关键。最早的传统可电离脂质,如 1,2-二油酰基-3-二甲基铵丙烷 (DODAP) 和 1,2-二油酰基-N,N-二甲基-3-氨基丙烷 (DODMA),是为了克服与永久电离相关的缺点而开发的。阳离子脂质系统中发现的带正电荷的化合物。使用这些可电离的脂质,可以有效地封装核酸并提供在生理pH值下具有接近中性电荷的LNP,由于其内体逃逸效率低,用于siRNA 递送的成功有限。人们合成了各种类型的可电离脂质,目的是通过改变早期可电离脂质 DODAP 和 DODMA 的化学结构来提高基因沉默效力。合成了一种高效脂MC3,它是第一个siRNA药物Patisiran的主要成分。
DNA的疫苗目前引起了人们的浓厚兴趣,因为与传统的肽疫苗相比,它们具有多种优势,包括快速且可重复的大规模生产,以及易于储存和运输。pDNA递送对于癌症疫苗特别有前景,它具有通过表达癌症抗原诱导抗原呈递和激活免疫细胞的潜力,并且其内在的佐剂作用导致触发细胞免疫。脾脏是基因疫苗靶器官的良好候选者,它含有多种类型的免疫细胞,可赋予先天性和适应性免疫。大多数静脉注射的含有包封核酸的LNP输送到肝脏和脾脏被降解,药物递送研究人员在将核酸输送到其他器官时通常专注于避免肝脏和脾脏的摄取。事实上,肝脏和脾脏是临床应用基因治疗的候选器官。
1.体内DODAP-LNPs 基因的高表达
作者做了Raw264.7细胞和小鼠动物实验来确定靶向脾脏的LNP,将YSK05-LNP与DODAP-LNPs做了对比。
结果表明:
(1)DODAP-LNPs转染Raw264.7细胞的效果低于YSK05-LNP(图1A)。
(2)DODAP-LNPs转染小鼠器官的效果高于YSK05-LNP,DODAP-LNPs具有较高的脾靶向能力(图1B)。
(3)进一步了解DODAP-LNP体内转染效果好的原因,做了两种LNP的表征分布(表1)。荧光素酶活性除以递送到每个组织的LNP量来计算基因表达效率。结果表明YSK-LNP优先递送至脾脏,递送量高于DODAP-LNP 。DODAP-LNP递送到肝脏的量高于脾脏(图1C)。
(4)生物分布结果不能解释YSK05-LNPs和DODAP-LNPs之间活性的差异。DODAP-LNPs在脾脏中的基因表达效率显着高于YSK05-LNPs。DODAP-LNPs是靶向脾脏的最佳候选(图1D)。
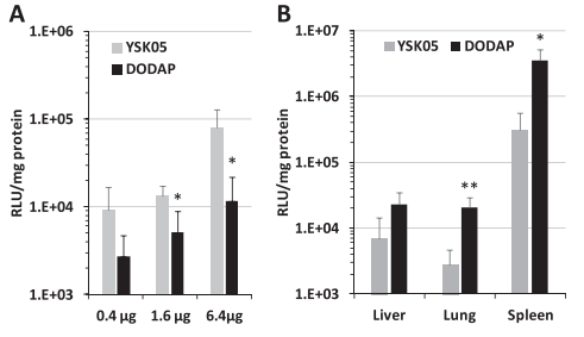
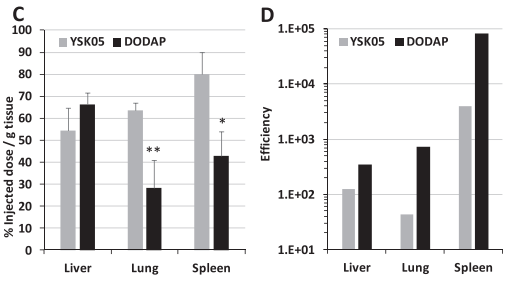
图1.YSK05-和DODAP-LNPs体外和体内转染活性的比较

2.DODAP-DOPE 组合是LNP靶向脾脏的关键因素
作者验证辅助脂质(DOPE)可能是 DODAP-LNP 的重要组成部分,选择(DOPE、二油酰磷酸胆碱(DOPC)或1-棕榈酰-2-油酰磷酸乙醇胺(POPE))制备了不同的DODAP-LNP。做了荧光素酶活性和生物分布实验。
结果表明:
(1)DOPE的LNP转染活性最高,脾脏靶向性最好(图2A)。
(2)三种LNP之间在脾脏递送量没有显著差异(图2B)。
(3)DODAP/DOPE组合在脾脏中基因表达效率远高于DODAP/POPE或DODAP/ DOPC, DODAP/POPE次之(图2C)。
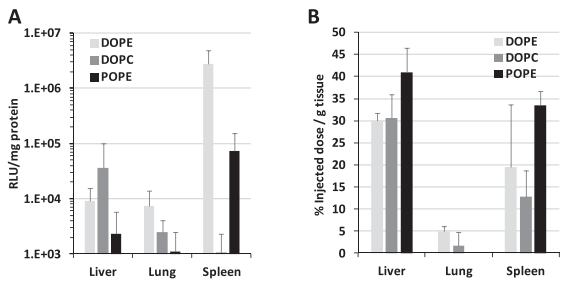
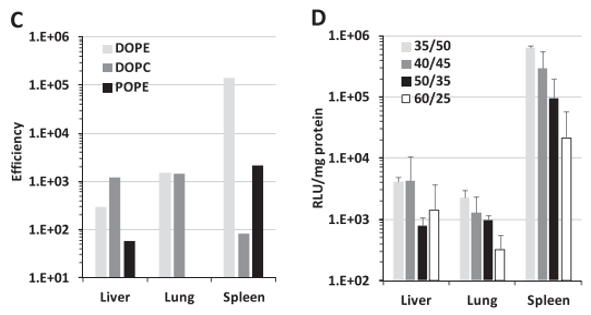
图2.使用不同辅助脂质和不同脂质比例制备的不同LNP的转染活性比较。
3.DODAP和DOPE的比例影响基因表达
作者对比了DODAP/DOPE 比率对LNP功能的影响,使用不同的DODAP/DOPE比例制备了不同的LNP。
结果表明:
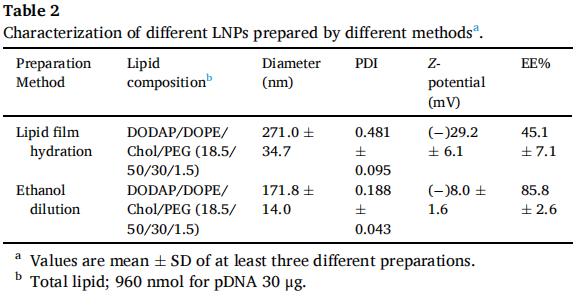
(1)对比了DODAP/DOPE比例在 35/50 至 60/25 范围内的影响发现与肝脏和肺脏相比,所有比例的LNP在脾脏都显示出最高活性,但随比例增加活性降低(图 2D)。
(2)比较了活性差异最大比例LNP的生物分布(DODAP/DOPE = 35/50 与 60/25),发现两中LNP生物分布无明显差异,但比例较低LNP的基因表达效率高(图 2E,F)。
(3)验证了DODAP/DOPE更广泛比例的活性,脾脏活性在15/70至35/50范围内达到上限, 15/70比率是脾/肝的最大活性比(图2G)。以上数据表明 DODAP 和 DOPE 的组合是LNP靶向脾脏的重要因素。为了扩大LNP的制备规模并获得更好的pDNA封装效率,比较了脂质膜水合与乙醇稀释。稀释法制备的LNP负电荷较低,pDNA封装较高,LNP更加均一(表2)。
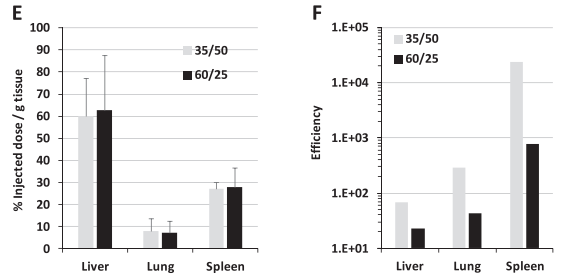
图2.使用不同辅助脂质和不同脂质比例制备的不同LNP的转染活性比较
4.验证靶向脾的LNP增强基因表达
作者使用离体成像检查了包括淋巴结在内的不同器官中的分布和基因表达(荧光素酶活性),确定乙醇稀释法制备的DODAP-DOPE-LNP靶向脾增强基因表达。
结果表明:
LNP主要分布在肝脏、肺和脾中。淋巴结在内的其他器官中观察少量荧光。脾脏显示出高基因表达,这证实了优化的LNP靶向脾增强了转染活性。

5.DODAP-DOPE-LNP 在抗原呈递细胞中的分布
作者检测了LNP分布到脾细胞的类型,确定基因高效表达的机制。使用特异性抗体来确定分布的脾细胞类型(T 细胞、B 细胞、DC 和巨噬细胞)
结果表明:
(1)优化后的DODAP-DOPE-LNPs主要分布于APC(抗原呈递细胞),如巨噬细胞、DC和B细胞。大部分荧光分布在B细胞(图4A)。
(2)DiD标记阳性细胞,90%巨噬细胞呈阳性,60%的B细胞呈阳性,40%的DC细胞呈阳性(图4B)。
(3)将LNP封装好的DNA注射到小鼠体内,收集脾脏,分离每种细胞测量荧光素酶活性(代表每个细胞的基因表达)。DODAP-LNP不转染T细胞,但有可能转染其他APC(图4C)。
(4)作者计算每种细胞类型的总基因表达量,脾脏中每种细胞类型的细胞数量(脾脏中每种细胞类型的百分比;T细胞:20-30%,B细胞:50-60% ,树突细胞:5%,巨噬细胞:5%)。脾脏中B细胞表达量最高(图4D)。
(5)为了证实脾脏中B细胞表达量最高,测量了脾脏中的总基因表达量。aCD20是阻断B细胞的抗体。B细胞损耗脾脏基因表达减少(图4E)。
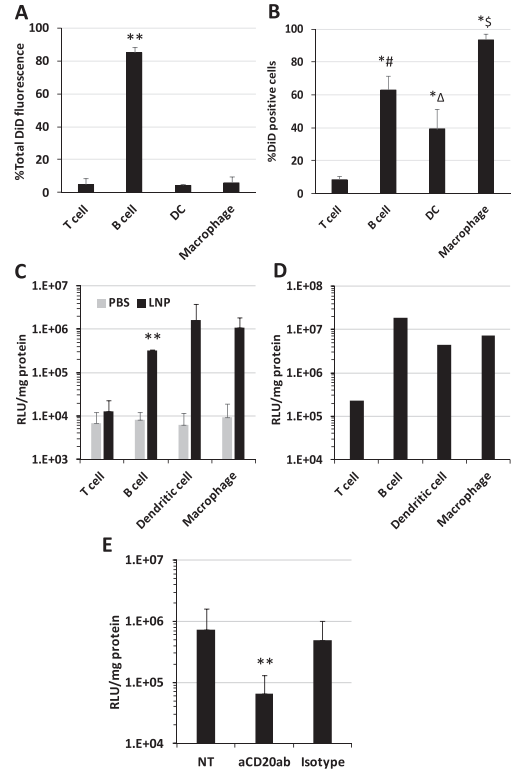
图4.DODAP/DOPE-LNP主要分布在抗原呈递细胞中
6.补体受体的摄取途径可能是脾脏活性高的关键因素
作者研究导致脾脏活性高的因素:据报道,与基于磷脂酰胆碱 (PC) 的脂质(例如 DOPC)相比,用基于磷脂酰乙醇胺 (PE) 的脂质(例如 DOPE 和 POPE)制备的脂质膜与补体3 (C3) 的结合更有效 。APC上表达的补体受体 (CR)。特异性抗体阻断 CD21/35 (CR1/2) 受体,在B细胞和巨噬细胞上表达,是脾脏中吸收DODAP-LNP的主要细胞(图4)。ICR小鼠在注射DODAP-LNP之前用抗CD21/35抗体处理以阻断CR。检测脾细胞的基因表达和LNP摄取。抗体介导的 CD21/35 阻断显着降低了脾脏中的基因表达和脾细胞的摄取,如图 5 所示。CR使脾脏的活性增高。脾细胞LNP摄取的减少可能是CR被阻断时导致活性降低,然而,这并不能解释转染活性的巨大差异,表明抗体处理不仅抑制了摄取,还抑制了一些细胞内过程。
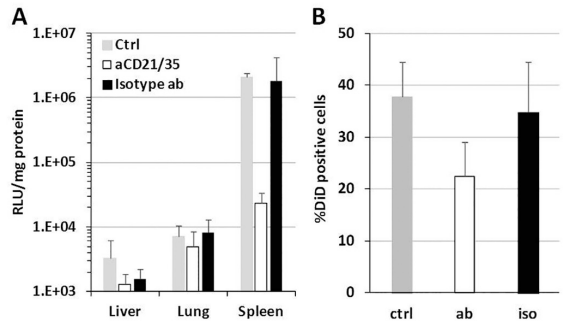
图5.CD21/35受体的摄取影响脾脏中基因表达和积累
7.DODAP-LNPs-pDNA抑制肿瘤生长
作者检测了DODAP-LNP的DNA疫苗预防性和治疗性抗肿瘤的效果。靶向脾载体DODAP-DOPE- pOVA、DODAP-DOPE-pLuc,对照PBS、pOVA、非靶向脾载体DODAP-DOPC-pOVA。预防性研究方面,小鼠接种肿瘤细胞前1周,注射LNP观察肿瘤体积。治疗性研究方面,小鼠接种肿瘤细胞后在第7天、10天和14天注射不同的LNP(图6)。结果显示:预防性方面,pOVA和DODAP-DOPC-pOVA都有抑制肿瘤生长的作用,DODAP-DOPE-pLuc和PBS组结果相当,与对照组PBS结果相比DODAP-DOPC-pOVA肿瘤抑制效果最佳(图6A)。治疗性方面,DODAP-DOPE-pOVA 显示肿瘤生长较慢,而其他对照与PBS治疗组相当(图 6B)。DODAP-DOPE-LNP是一种有效的靶向脾载体,其在APC中表达抗原并诱靶向肿瘤的特异性免疫反应。


图6.包封抗原(OVA)编码pDNA的不同DODAP-LNP预防和治疗抗肿瘤作用
8.免疫反应分析
检测了DODAP-LNP治疗后的免疫反应,结果表明:注射后2h和6h血清结果发现IL-6、IFN-α、β、IFN-γ的LNP-pLuc和LNP-pOVA可诱导更高的血清细胞因子产生,pDNA或PBS为对照(图7A)。IL-6、IFN-γ和IFN-α做了抗原特异性细胞毒作用和抗原特异性抗体产生实验。结果表明:含有非特异性CPG的pLuc质粒比不含CPG的pOVA质粒产生更高的细胞因子。
LNP-pOVA产生强OVA特异性细胞毒性T淋巴细胞(CTL)活性和强OVA特异性IgG抗体滴度(图7B,C)。验证了B细胞参与抗肿瘤免疫反应,在存在或不存在特异性抗体的情况下测量OVA特异性CTL活性和OVA特异性IgG抗体滴度(aCD20),aCD20会消耗B细胞。aCD20抗体的显着降低CTL活性和抗体产生(图7D,E),表明B淋巴细胞是负责免疫反应的主要细胞,无论是先天性免疫还是适应性免疫。结果表明,脾脏中的B细胞是肿瘤特异性免疫刺激的重要靶标。
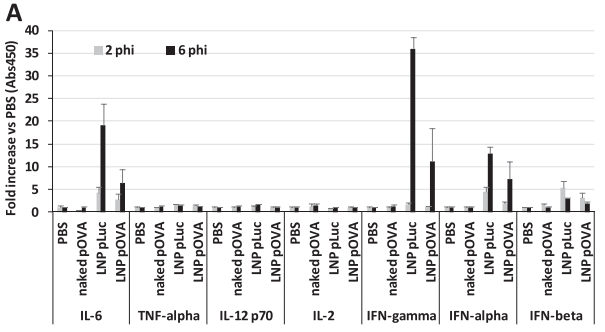
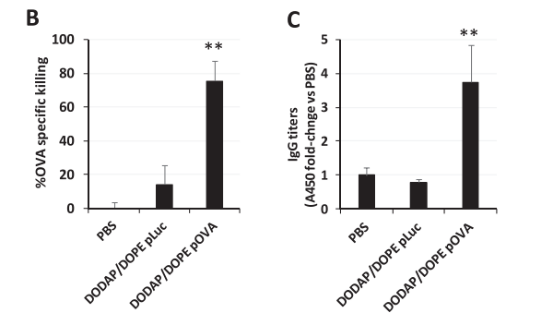
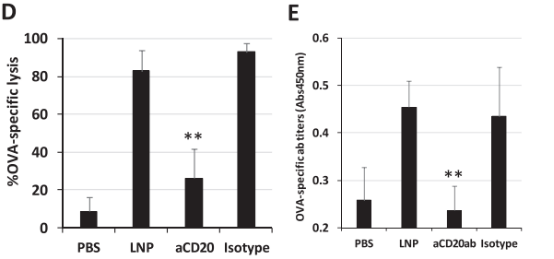
图7.免疫反应分析
综上所述,作者报告了一种新型脂质组合,可实现pDNA有效的靶向脾脏的基因递送。这种脂质组合主要由DODAP和常见的辅助脂质组成;DODAP/DOPE-LNPs靶向脾脏基因表达效果显著,目前是递送基因的最佳组合。包封编码pDNA的LNP抗原有预防性和治疗性抗肿瘤作用。基恩科致力于研发LNP递送pDNA的产品,将会提供LNP递送pDNA的技术服务及现货产品,敬请期待!